Globaler Markt für Unterstützungsleistungen in klinischen Studien: Nach Studientyp (zentralisierte und dezentralisierte klinische Studien); Therapieart (niedermolekulare Wirkstoffe, Biologika, medizinische Therapien); Phasen (präklinische Studien, Phase I, Phase II, Phase III und Phase IV); Dienstleistungen (Standortmanagement, Patientenrekrutierung, Studienmanagement, Datenmanagement, Sonstige); Anwendung (Onkologie, ZNS- und psychische Erkrankungen, Herz-Kreislauf-Erkrankungen, Infektionskrankheiten, Blutkrankheiten, Sonstige); Endnutzer (Pharma- und Biotechnologieunternehmen, Auftragsforschungsinstitute (CROs), Unternehmen im Bereich medizinischer Therapien, Sonstige); Regional – Marktgröße, Branchendynamik, Chancenanalyse und Prognose für 2024–2032
- Letzte Aktualisierung: 26. Februar 2024 | | Bericht-ID: AA0923622
Marktszenario
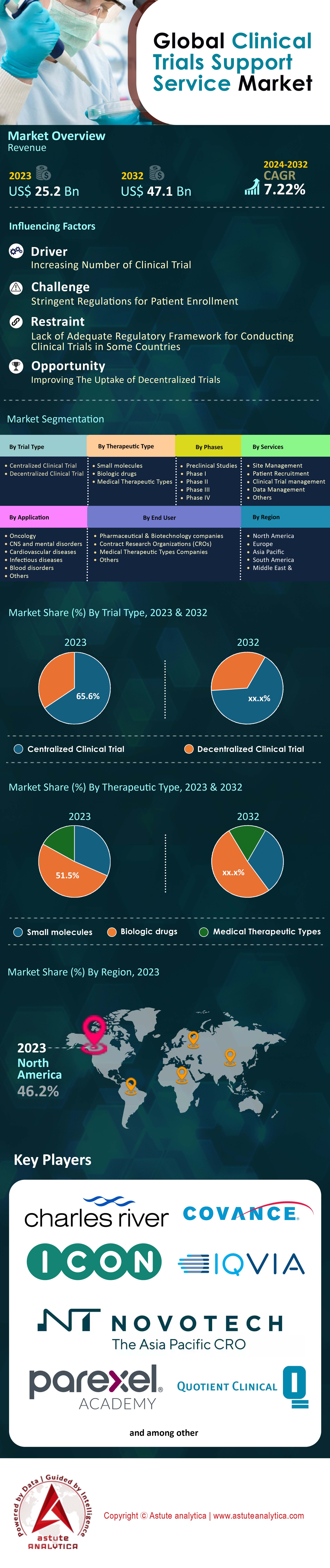
Der globale Markt für Unterstützungsleistungen für klinische Studien im Jahr 2023 auf 25,2 Milliarden US-Dollar geschätzt und soll bis 2032 auf über 47,1 Milliarden US-Dollar , was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 7,22 % im Prognosezeitraum 2024–2032 entspricht.
Der Markt für Unterstützungsleistungen für klinische Studien ist ein unverzichtbares Rückgrat des globalen Gesundheitswesens. Er spielt eine entscheidende Rolle bei der Entwicklung innovativer Behandlungen und bahnbrechender Therapien. Angesichts der weltweit zunehmenden Zahl von Krankheiten und Beschwerden liegt der Fokus verstärkt auf der Entwicklung neuerer, sichererer und wirksamerer Behandlungen. Diese Entwicklung hat die Nachfrage nach umfassenden und effizienten Unterstützungsleistungen für klinische Studien deutlich erhöht. Die CDC hob in ihren jüngsten Veröffentlichungen den Anstieg klinischer Studien hervor, insbesondere im Bereich der Infektionskrankheiten. Dieser Anstieg ist auf die aktuellen globalen Herausforderungen im Gesundheitswesen zurückzuführen, die eine rasche Forschung und die Entwicklung von Lösungen erforderlich machten. Der Fokus liegt nicht nur auf der Medikamentenentwicklung, sondern auch auf dem Verständnis der Langzeitwirkungen und möglichen Komplikationen von Krankheiten, was die Nachfrage nach umfassender Unterstützung für klinische Studien weiter ankurbelt.
Die FDA, eine weitere wichtige Behörde für die Zulassung von Arzneimitteln und die Durchführung klinischer Studien in den USA, meldete einen Anstieg der Neuzulassungsanträge (NDA) um 15 % im vergangenen Jahr. Dieser Anstieg zeugt zwar von der florierenden Pharmaindustrie , unterstreicht aber auch den wachsenden Bedarf an Unterstützungsleistungen für klinische Studien. Mit jedem neuen Arzneimittel oder Therapieantrag fallen enorme Datenmengen an, die verarbeitet, verwaltet und analysiert werden müssen, wodurch die Rolle dieser Unterstützungsleistungen unverzichtbar wird.
Ein bemerkenswerter Trend im Markt für Unterstützungsleistungen klinischer Studien ist die zunehmende Patientenorientierung. Die FDA betont die Bedeutung von patientenberichteten Ergebnissen, was die Studien zusätzlich komplexer macht. Dienstleistungen, die die Rekrutierung und Bindung von Patienten sowie die Erfassung von Daten aus dem realen Versorgungsalltag unterstützen, gewinnen an Bedeutung. Diese Entwicklung hat zu einem sprunghaften Anstieg der Nachfrage nach spezialisierten Unterstützungsleistungen geführt und den Markt weiter angekurbelt. Nordamerika, insbesondere die USA, bleibt regional ein wichtiger Akteur im Markt für klinische Studien. Der asiatisch-pazifische Raum, angeführt von Ländern wie China und Indien, entwickelt sich jedoch rasant zu einem Zentrum für klinische Forschung. Dieser Wandel wird durch das Zusammenspiel von qualifizierten Fachkräften, fortschrittlicher Infrastruktur und günstigen regulatorischen Rahmenbedingungen begünstigt. Laut aktuellen Berichten verzeichnete der asiatisch-pazifische Raum ein Wachstum von 9 % bei klinischen Studien und übertraf damit den globalen Durchschnitt.
Für weitere Einblicke fordern Sie ein kostenloses Muster an.
Marktdynamik
Treiber: Technologische Fortschritte in der Datenanalyse und künstlichen Intelligenz
Die Integration fortschrittlicher Datenanalyse und künstlicher Intelligenz (KI) hat sich zu einem entscheidenden Wachstumstreiber im Markt für Unterstützungsleistungen klinischer Studien entwickelt. Traditionell basierten klinische Studien auf manuellen Verfahren, doch die heutige Situation ist von signifikanten technologischen Fortschritten geprägt. So wurde beispielsweise geschätzt, dass eine einzelne Phase-III-Studie im Jahr 2022 über 3 Terabyte an Daten generieren würde. Da Prognosen einen jährlichen Anstieg dieser Datenmenge um 10 % bis 2025 vorhersagen, ist das schiere Datenvolumen enorm.
Angesichts dieser rasant wachsenden Datenmengen haben KI-gestützte Tools und fortschrittliche Analysen einen tiefgreifenden Wandel bewirkt. Bis 2025 werden voraussichtlich über 65 % der Dienstleister für klinische Studien KI oder ähnliche fortschrittliche Analysemethoden einsetzen. Dies sind nicht nur technologische Vorteile, sondern haben auch finanzielle Auswirkungen. Die potenziellen Kosteneinsparungen durch den Einsatz von KI-Tools in der Arzneimittelentwicklung liegen zwischen 15 und 20 %. Da die durchschnittlichen Entwicklungskosten für ein neues verschreibungspflichtiges Medikament, das die Marktzulassung für klinische Studien erhält, im Jahr 2021 bei rund 2,6 Milliarden US-Dollar lagen, beläuft sich das Kosteneinsparungspotenzial von KI auf Milliarden.
Darüber hinaus hat die KI-gestützte prädiktive Analytik die Dynamik der Entscheidungsfindung in der Arzneimittelentwicklung grundlegend verändert. Früher dauerte die Entscheidung über die Machbarkeit eines Arzneimittelpfads Monate. Dank KI werden solche Entscheidungen nun innerhalb von Wochen oder sogar Tagen getroffen. Eine Studie zeigte, dass fast 70 % der Pharmaunternehmen, die KI einsetzen, ihre Entscheidungszeiten halbieren konnten.
Trend: Verstärkte Betonung der Patientendiversität in klinischen Studien
Ein prominenter Trend, der im Markt für Unterstützungsleistungen klinischer Studien zunehmend an Bedeutung gewinnt, ist die verstärkte Betonung der Patientendiversität. Vor einigen Jahren stand Diversität in klinischen Studien noch nicht im Vordergrund. Im Jahr 2019 gaben jedoch nur etwa 20 % der klinischen Studien an, eine diverse Patientenbasis zu haben. Bis 2022 stieg diese Zahl sprunghaft auf 35 %. Diese Entwicklung lässt vermuten, dass bis 2025 über die Hälfte der neuen klinischen Studien der Patientendiversität Priorität einräumen werden. Regulierungsbehörden haben diesen Trend maßgeblich beeinflusst. So sorgte beispielsweise die Veröffentlichung von Leitlinien der FDA im Jahr 2020, die die Notwendigkeit von Patientendiversität in klinischen Studien unterstrichen, für Aufsehen in der Branche. Nach Veröffentlichung dieser Leitlinien gaben rund 40 % der Pharmaunternehmen an, ihre Rekrutierungsstrategien überarbeitet zu haben, um eine breitere und diversere Teilnehmerbasis zu gewährleisten.
Diversität in klinischen Studien ist nicht nur eine Frage der Repräsentation, sondern auch eine wirtschaftlich sinnvolle Strategie. Medikamente, die an einer vielfältigeren Patientengruppe getestet werden, stoßen in der Regel auf weniger Hürden im Zulassungsverfahren, was zu einem schnelleren Marktzugang im Bereich der klinischen Studienunterstützung führt. Schätzungen zufolge können Unternehmen, die auf diverse Studien setzen, die Markteinführungszeit ihrer Medikamente um bis zu sechs Monate verkürzen. Dies kann potenziell zu einer Umsatzsteigerung von 10–15 % führen. Darüber hinaus hat die Fokussierung auf Diversität einen weiteren, schwer fassbaren, aber dennoch tiefgreifenden Effekt: Sie schafft Vertrauen. Historisch unterrepräsentierte Bevölkerungsgruppen standen der klinischen Forschung oft skeptisch gegenüber. Eine Umfrage aus dem Jahr 2022 zeigte jedoch, dass 60 % der Befragten aus diesen Gruppen eher bereit wären, an klinischen Studien teilzunehmen, wenn sie über das Engagement der Studie für Diversität informiert wären.
Herausforderung: Datenschutz- und Sicherheitsbedenken in klinischen Studien
Im globalen Markt für Unterstützungsleistungen klinischer Studien sticht eine Herausforderung besonders hervor: die Gewährleistung von Datenschutz und Datensicherheit. Da klinische Studien zunehmend auf digitale Plattformen verlagert werden, sind die großen Mengen an sensiblen Patientendaten einem erhöhten Risiko von Datenschutzverletzungen und unbefugtem Zugriff ausgesetzt. Die Umstellung auf elektronische Patientenakten und digitale Datenerfassungstools hat zwar die Effizienz gesteigert, aber gleichzeitig die Anfälligkeit des Systems erhöht. So wurde beispielsweise im Jahr 2021 ein Anstieg der Cyberangriffe auf Gesundheitsdaten um 30 % im Vergleich zum Vorjahr verzeichnet. Solche Angriffe gefährden nicht nur die Integrität der Studie, sondern riskieren auch die Privatsphäre der Studienteilnehmer und können deren persönliche Gesundheitsdaten offenlegen.
Die globale Ausrichtung vieler klinischer Studien bringt zusätzliche Komplexität mit sich. Verschiedene Länder haben ihre eigenen Vorschriften und Standards zum Datenschutz. Die Navigation durch diese unterschiedlichen regulatorischen Rahmenbedingungen kann für Pharmaunternehmen und Organisatoren klinischer Studien eine Herausforderung darstellen. Eine Studie aus dem Jahr 2022 ergab, dass fast 40 % der internationalen klinischen Studien aufgrund von Diskrepanzen bei den Datenschutzstandards zwischen den Ländern auf regulatorische Hürden stießen. Die Auswirkungen dieser Herausforderungen sind vielfältig. Vertrauen, die Grundlage für die Teilnahme von Patienten an klinischen Studien, steht auf dem Spiel. Wenn Teilnehmer befürchten, dass ihre Daten gefährdet sein könnten, sind sie weniger geneigt, sich anzumelden, was den Fortschritt potenziell lebensrettender Forschung behindern kann. Im Zeitalter der digitalen Transformation bleibt die Gewährleistung eines robusten Datenschutzes und der Datensicherheit eine zentrale Herausforderung für den globalen Markt für Unterstützungsleistungen im Bereich klinischer Studien.
Segmentanalyse
Nach Art der Verhandlung:
Gemessen an der Studienart nimmt das Segment der zentralisierten klinischen Studien im globalen Markt für Unterstützungsleistungen für klinische Studien eine herausragende Stellung ein. Mit einem beachtlichen Marktanteil von 65,6 % dominiert es diesen Bereich deutlich. Traditionell spielen zentralisierte klinische Studien eine zentrale Rolle in der Forschung und bieten Vorteile in Bezug auf standardisierte Protokolle, einheitliche Datenerfassungsmethoden und optimierte Kommunikationswege.
Das Segment der zentralisierten klinischen Studien wird im Prognosezeitraum voraussichtlich mit einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 7,41 % am schnellsten wachsen. Sollten sich diese Prognosen bewahrheiten, könnte der Marktanteil dieses Segments bis zum Ende des Jahrzehnts potenziell fast 70 % erreichen und seine führende Position weiter festigen. Das beschleunigte Wachstum ist auf die zunehmende Komplexität der Studien, die Zunahme multiregionaler klinischer Studien und die Vorteile zentralisierter Studien hinsichtlich Kosteneffizienz und Zeitersparnis zurückzuführen.
Nach Therapieart:
Im therapeutischen Bereich zeigt der Markt eine deutliche Tendenz zu Biologika. Mit einem beeindruckenden Marktanteil von 51,5 % haben sich Biologika zum Rückgrat des globalen Marktes für Unterstützungsleistungen in klinischen Studien entwickelt. Aufgrund ihrer komplexen Natur und ihres Potenzials zur Behandlung eines breiten Spektrums von Krankheiten, von Autoimmunerkrankungen bis hin zu Krebs, haben Biologika ein stark gestiegenes Forschungsinteresse und erhebliche Investitionen erfahren.
Darüber hinaus scheint sich dieser Trend in absehbarer Zeit nicht abzuschwächen. Biologika, die dem Wachstumsmuster zentralisierter klinischer Studien entsprechen, werden voraussichtlich jährlichen Wachstumsrate (CAGR) von 7,41 % . Dieses stetige Wachstum im Biologika-Segment wird durch eine Vielzahl von Faktoren angetrieben. Das zunehmende Verständnis der Genetik, der Aufstieg der personalisierten Medizin und die kontinuierlichen Fortschritte in der Biotechnologie sind nur einige der Katalysatoren, die Biologika in den Mittelpunkt der therapeutischen Forschung rücken.
Nach Phasen:
Im globalen Markt für Unterstützungsleistungen in klinischen Studien dominiert Phase III mit einem Marktanteil von 48 %. Diese starke Stellung ist auf die entscheidende Bedeutung von Phase-III-Studien in der Arzneimittelentwicklung zurückzuführen. Diese Studien, oft auch als Zulassungsstudien bezeichnet, umfassen eine große Teilnehmergruppe und sind maßgeblich für die Beurteilung der Wirksamkeit und potenzieller Nebenwirkungen der jeweiligen Behandlung. Aufgrund ihres Umfangs und ihrer Komplexität erfordern Phase-III-Studien umfangreiche Ressourcen, Überwachung und Management, was einen erheblichen Anteil der Unterstützungsleistungen ausmacht.
Ein weiterer Faktor, der die Bedeutung der Phase III unterstreicht, ist ihre regulatorische Relevanz. Der erfolgreiche Abschluss dieser Phase bildet oft die Grundlage für die Zulassung durch Behörden wie die FDA oder die EMA. Da Arzneimittelentwickler sicherstellen wollen, dass ihre Prüfpräparate diese Phase mit eindeutig positiven Ergebnissen abschließen, sind die Investitionen in unterstützende Dienstleistungen für Phase III naturgemäß hoch.
Diesen Bericht anpassen + von einem Experten validieren
Greifen Sie nur auf die Abschnitte zu, die Sie benötigen – regionsspezifisch, unternehmensbezogen oder nach Anwendungsfall.
Beinhaltet eine kostenlose Beratung mit einem Domain-Experten, der Sie bei Ihrer Entscheidung unterstützt.
Um mehr über diese Studie zu erfahren: Fordern Sie ein kostenloses Muster an
Nach Dienstleistungen:
Im globalen Markt für Unterstützungsleistungen klinischer Studien sticht das Segment des klinischen Studienmanagements mit einem beeindruckenden Marktanteil von 54 % hervor. Klinisches Studienmanagement umfasst eine Reihe essenzieller Dienstleistungen, von der Patientenrekrutierung über die Standortauswahl und das Datenmanagement bis hin zur Einhaltung regulatorischer Vorgaben und der Berichterstattung. Angesichts der Komplexität moderner klinischer Studien mit ihren vielschichtigen Protokollen, heterogenen Patientenpopulationen und strengen regulatorischen Anforderungen ist ein effektives Management unerlässlich.
Die Dominanz des Segments „Management klinischer Studien“ lässt sich auch auf die zunehmende Globalisierung klinischer Studien zurückführen. Da Studien an mehreren Standorten, oft in verschiedenen Ländern oder Kontinenten, durchgeführt werden, besteht ein deutlicher Bedarf an zentralisiertem Management, um Einheitlichkeit und die Einhaltung von Standards zu gewährleisten. Diese Nachfrage nach nahtlosem, koordiniertem Management über geografisch verteilte Standorte hinweg lenkt Investitionen und die Abhängigkeit naturgemäß auf Dienstleistungen im Bereich des Managements klinischer Studien.
Da sich die Branche zunehmend patientenzentrierten Ansätzen und Real-World-Daten zuwendet, haben sich die Feinheiten des klinischen Studienmanagements erweitert, was die Bedeutung dieses Dienstleistungssegments im globalen Markt für Unterstützungsleistungen im Bereich klinischer Studien weiter unterstreicht. Die Sicherstellung der Patienten-Compliance, die Integration von Real-World-Daten und die Nutzung digitaler Tools sind heute integrale Bestandteile des Studienmanagements und erfordern spezialisierte Unterstützungsleistungen.
Regionalanalyse
Nordamerika ist unbestrittener Marktführer im Bereich der Unterstützung klinischer Studien und erzielt einen beeindruckenden Umsatzanteil von 46,2 %. Die Dominanz der Region ist maßgeblich auf die Vereinigten Staaten zurückzuführen, die seit jeher ein Zentrum bahnbrechender medizinischer Forschung und Innovation sind. Mit einer Vielzahl global anerkannter Forschungseinrichtungen und Pharmaunternehmen verzeichnet die Region einen signifikanten Zufluss an Investitionen in die klinische Forschung. Allein im Jahr 2021 stellten die National Institutes of Health (NIH) über 41 Milliarden US-Dollar für die medizinische Forschung bereit. Diese leistungsstarke Forschungsinfrastruktur, gepaart mit den strengen regulatorischen Anforderungen der Food and Drug Administration (FDA), erfordert ein breites Spektrum spezialisierter Unterstützungsleistungen, um die Einhaltung der Vorschriften, die Effizienz und die Qualität klinischer Studien zu gewährleisten. Darüber hinaus hat der Aufstieg neuer Therapiegebiete wie der Präzisionsmedizin und der Gentherapie die Anzahl klinischer Studien in der Region um schätzungsweise 8 % pro Jahr erhöht und damit die Nachfrage nach Unterstützungsleistungen weiter angeheizt.
Der europäische Markt für Unterstützungsleistungen im Bereich klinischer Studien behauptet sich als bedeutender Akteur und hält über 26 % Marktanteil. Die europäische Landschaft zeichnet sich durch ihre vielfältige Demografie und Patientenpopulation aus und bietet damit einen einzigartigen Vorteil für klinische Studien mit dem Ziel allgemeingültiger Ergebnisse. Im Geschäftsjahr 2021/22 investierten Länder wie Deutschland, Frankreich und Großbritannien zusammen 15 Milliarden Euro in die klinische Forschung, was das Engagement der Region für den Fortschritt der medizinischen Wissenschaft unterstreicht. Die Attraktivität Europas wird zusätzlich durch die Europäische Arzneimittel-Agentur (EMA) und ihre kontinuierlichen Bemühungen um eine Harmonisierung der regulatorischen Vorgaben in den Mitgliedstaaten gestärkt. Diese Initiativen haben die ehemals mit multinationalen Studien verbundenen bürokratischen Hürden in der Region deutlich reduziert. Infolgedessen verzeichnet die Nachfrage nach Unterstützungsleistungen für klinische Studien in Europa ein stetiges jährliches Wachstum von rund 6 %.
Führende Akteure auf dem globalen Markt für Unterstützungsleistungen für klinische Studien
- Charles River Laboratories
- Covance Inc.
- Icon PLC
- inVentiv International Pharma Services
- IQVIA
- Laboratory Corp. of America Holdings
- Novotech
- Parexel International
- Pharmaceutical Product Development LLC
- Quotient Bioresearch
- WuXi AppTec
- Leukemia & Lymphoma Society (LLS)
- Weitere prominente Spieler
Marktsegmentierungsübersicht:
Nach Versuchsart
- Zentralisierte klinische Studie
- Dezentrale klinische Studie
Nach Therapieart
- Kleine Moleküle
- Biologische Arzneimittel
- Medizinische Therapiearten
Nach Phasen
- Präklinische Studien
- Phase I
- Phase II
- Phase III
- Phase IV
Nach Dienstleistungen
- Standortverwaltung
- Patientenrekrutierung
- Management klinischer Studien
- Datenmanagement
- Andere
Durch Bewerbung
- Onkologie
- ZNS- und psychische Störungen
- Herz-Kreislauf-Erkrankungen
- Infektionskrankheiten
- Blutkrankheiten
- Andere
Vom Endbenutzer
- Pharma- und Biotechnologieunternehmen
- Auftragsforschungsinstitute (CROs)
- Unternehmen für medizinische Therapiearten
- Andere
Nach Region
- Nordamerika
- Die USA
- Kanada
- Mexiko
- Europa
- Großbritannien.
- Deutschland
- Frankreich
- Spanien
- Polen
- Belgien
- Finnland
- Niederlande
- Portugal
- Schweden
- Schweiz
- Restliches Europa
- Asien-Pazifik
- China
- Indien
- Japan
- Australien und Neuseeland
- ASEAN
- Südkorea
- Übriges Asien-Pazifik
- Naher Osten und Afrika
- VAE
- Saudi-Arabien
- Katar
- Südafrika
- Marokko
- Rest von MEA
- Südamerika
- Brasilien
- Argentinien
- Kolumbien
- Chile
- Peru
- Restliches Südamerika
BERICHTSUMFANG
| Berichtattribute | Details |
|---|---|
| Marktgröße im Jahr 2023 | 25,2 Milliarden US-Dollar |
| Erwartete Einnahmen im Jahr 2032 | 47,1 Milliarden US-Dollar |
| Historische Daten | 2019-2022 |
| Basisjahr | 2023 |
| Prognosezeitraum | 2024-2032 |
| Einheit | Wert (Mrd. USD) |
| CAGR | 7.22% |
| Abgedeckte Segmente | Nach Studientyp, Therapieart, Phasen, Dienstleistungen, Anwendung, Endnutzer, Region |
| Wichtige Unternehmen | Charles River Laboratories, Covance Inc., Icon PLC, inVentiv International Pharma Services, IQVIA, Laboratory Corp. of America Holdings, Novotech, Parexel International, Pharmaceutical Product Development LLC, Quotient Bioresearch, WuXi AppTec, Leukemia & Lymphoma Society (LLS) und weitere bedeutende Akteure |
| Anpassungsumfang | Erhalten Sie Ihren individuell angepassten Bericht nach Ihren Wünschen. Fragen Sie nach individuellen Anpassungen. |
SIE SUCHEN UMFASSENDES MARKTWISSEN? KONTAKTIEREN SIE UNSERE EXPERTEN.
SPRECHEN SIE MIT EINEM ANALYSTEN
.svg)