全球临床试验支持服务市场:按试验类型(集中式临床试验和分散式临床试验);治疗类型(小分子药物、生物制剂、传统药物);阶段(临床前研究、I期、II期、III期和IV期);服务(现场管理、患者招募、临床试验管理、数据管理及其他);应用领域(肿瘤、中枢神经系统和精神疾病、心血管疾病、传染病、血液疾病及其他);最终用户(制药和生物技术公司、合同研究组织 (CRO)、传统药物公司及其他);区域市场规模、行业动态、机遇分析及2024-2032年预测
- 最后更新日期:2024年2月26日 | | 报告编号:AA0923622
市场概况
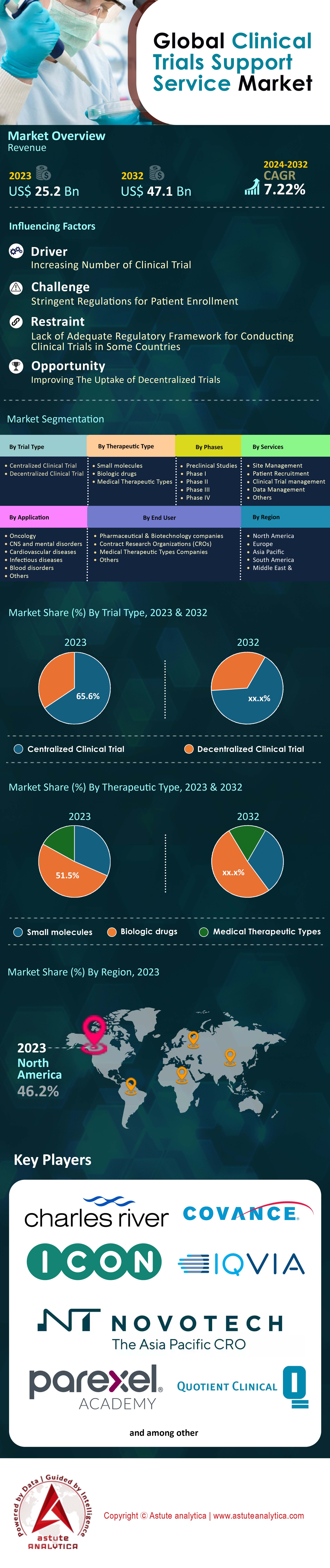
全球 临床试验支持服务市场 价值为 252 亿美元 ,预计 到 2032 年将超过 471 亿美元, 复合 年增长率为 7.22% 在 2024 年至 2032 年的预测期内, 。
临床试验支持服务市场是全球医疗保健行业的重要支柱。它在推动创新疗法和突破性治疗方面发挥着关键作用。随着全球各种疾病和病症的激增,人们越来越重视开发更新、更安全、更有效的治疗方法。这种需求显著提升了对强大且高效的临床试验支持服务的需求。美国疾病控制与预防中心(CDC)在其近期发布的报告中强调了临床试验数量的激增,尤其是在传染病领域。这一激增可归因于近期全球面临的健康挑战,这些挑战迫切需要快速开展研究和开发解决方案。研究的重点不仅在于药物研发,还在于了解疾病的长期影响和潜在并发症,这进一步推动了对长期临床试验支持服务的需求。.
美国食品药品监督管理局(FDA)是美国另一个负责药品审批和临床试验的关键机构。该机构报告称,过去一年新药申请(NDA)数量增长了15%。这一增长不仅表明 制药行业的,也凸显了对临床试验支持服务日益增长的需求。每项新药或疗法申请都会产生大量数据需要处理、管理和分析,因此这些支持服务的作用不可或缺。
临床试验支持服务市场的一个显著趋势是向以患者为中心的试验模式转变。美国食品药品监督管理局 (FDA) 一直强调患者报告结局的重要性,这为试验增添了新的复杂性。能够帮助患者招募、留存和收集真实世界数据的服务正日益受到重视。这种转变导致对专业支持服务的需求激增,进一步推动了市场发展。从区域来看,北美(主要是美国)仍然是临床试验市场的重要参与者。然而,以中国和印度等国家为首的亚太地区正在迅速崛起为临床研究中心。这一转变得益于熟练的劳动力、先进的基础设施和有利的监管环境。根据最新报告,亚太地区的临床试验增长率达到 9%,超过了全球平均水平。.
如需了解更多信息, 请申请免费样品
市场动态
驱动因素:数据分析和人工智能领域的技术进步
先进数据分析和人工智能 (AI) 的融合已成为推动临床试验支持服务市场发展的重要驱动力。以往,临床试验主要依赖人工操作,但如今已取得了显著的技术进步。例如,据估计,2022 年一项 III 期临床试验产生的数据量将超过 3 TB。预计到 2025 年,此类数据量将以每年 10% 的速度增长,其庞大的数据量将令人震惊。.
为了应对海量数据,人工智能和高级分析工具发挥了变革性作用。预计到2025年,超过65%的临床试验支持服务将在其运营中采用人工智能或类似的高级分析技术。这不仅是技术上的福音,也具有重要的经济意义。在药物研发过程中应用人工智能工具,潜在的成本节约可达15%至20%。鉴于2021年开发一种获得临床试验支持服务市场批准的新处方药的平均成本约为26亿美元,人工智能的潜在成本节约额高达数十亿美元。.
此外,人工智能驱动的预测分析改变了药物研发决策的格局。过去,评估药物研发路径的可行性需要数月时间。但随着人工智能的出现,如今这类决策只需几周甚至几天即可完成。一项研究表明,近70%使用人工智能的制药公司成功地将决策时间缩短了一半。.
趋势:临床试验中越来越重视患者多样性
临床试验支持服务市场的一个显著趋势是,对患者多样性的日益重视。几年前,临床试验中的多样性并非首要关注点。然而,2019年,仅有约20%的临床试验报告称其患者群体具有多样性。到2022年,这一数字跃升至35%。这一趋势表明,到2025年,我们可能会看到超过一半的新临床试验将患者多样性放在首位。监管机构对这一趋势产生了显著影响。例如,美国食品药品监督管理局(FDA)于2020年发布指南,强调临床试验中患者多样性的必要性,这在业内引起了广泛关注。指南发布后,约40%的制药公司表示已调整其招募策略,以确保更广泛、更多样化的受试者群体。.
临床试验中的多样性不仅关乎代表性,更是一项经济有效的策略。在更多元化的患者群体中进行测试的药物,在监管审批过程中遇到的障碍可能更少,这意味着在临床试验支持服务市场,药物能够更快地进入市场。据估计,重视多样性试验的公司可以将药物上市时间缩短多达六个月,从而潜在地提高10%至15%的收入。此外,关注多样性还有另一个无形却意义深远的影响:建立信任。历史上代表性不足的群体往往对临床研究持怀疑态度。然而,2022年的一项调查显示,如果这些群体中的受访者了解试验对多样性的承诺,他们将更愿意参与临床试验。.
挑战:临床试验中的数据隐私和安全问题
在全球临床试验支持服务市场中,一项挑战尤为突出:确保数据隐私和安全。随着临床试验逐步向数字化平台转移,产生的大量敏感患者数据面临着更高的泄露和未经授权访问风险。电子健康记录和数字数据采集工具的普及虽然提高了效率,但也加剧了系统的脆弱性。例如,据报道,2021年针对医疗保健数据的网络攻击比上一年增加了30%。此类攻击不仅会危及试验的完整性,还会威胁参与者的隐私,可能导致其个人健康信息泄露。.
许多临床试验的全球性也带来了另一层复杂性。不同国家/地区对于数据隐私有着各自的法规和标准。对于制药公司和临床试验组织者而言,应对这些不同的监管环境可能充满挑战。2022 年的一项研究发现,近 40% 的国际临床试验由于各国数据隐私标准的差异而面临监管障碍。这些挑战的影响是多方面的。信任是患者参与临床试验的基石,而信任正受到威胁。如果参与者认为他们的数据可能面临风险,他们参与的意愿就会降低,这可能会阻碍可能拯救生命的研究进展。在数字化转型时代,确保强大的数据隐私和安全仍然是全球临床试验支持服务市场面临的一项关键挑战。.
细分市场分析
按试验类型:
按试验类型划分,集中式临床试验在全球临床试验支持服务市场中占据显著地位。其市场份额高达65.6%,在该领域占据绝对主导地位。长期以来,集中式临床试验在研究领域一直发挥着关键作用,其优势在于标准化的试验方案、统一的数据收集方法以及简化的沟通渠道。.
快速增长 7.41%的复合年增长率。如果这些预测成真,到本十年末,该领域的市场份额有望接近70%,进一步巩固其领先地位。加速增长可归因于试验复杂性的增加、多区域临床试验的兴起,以及集中式试验在成本效益和时间效率方面的优势。
按治疗类型:
在治疗领域,市场明显偏向生物制剂。生物制剂占据了高达51.5%的市场份额,已成为全球临床试验支持服务市场的中流砥柱。鉴于生物制剂的复杂性及其治疗范围广泛(从自身免疫性疾病到癌症)的潜力,其研究兴趣和投资激增。.
此外,这一趋势似乎短期内不会趋于平缓。生物制剂的增长模式与集中式临床试验领域类似,预计 7.41%的复合年增长率(CAGR) 。生物制剂领域的持续增长是由诸多因素推动的。对遗传学认识的不断加深、个性化医疗的兴起以及生物技术的持续进步,仅仅是推动生物制剂成为治疗研究前沿的几个催化剂。
按阶段:
按试验阶段划分,III期临床试验在全球临床试验支持服务市场占据主导地位,市场份额高达48%。这一显著优势可归因于III期临床试验在药物研发流程中的关键性。这些试验通常被称为关键性研究,涉及更大规模的受试者群体,对于评估目标疗法的疗效和潜在副作用至关重要。鉴于III期临床试验的规模和复杂性,它们需要大量的资源、监测和管理,因此也催生了相当一部分支持服务。.
另一个强化三期临床试验主导地位的因素是其监管重要性。成功完成三期临床试验往往是获得FDA或EMA等监管机构批准的基石。由于药物研发者力求确保其在研疗法能够顺利通过三期临床试验并取得明确的积极结果,因此对三期临床试验支持服务的投入自然很高。.
自定义此报告 + 与专家验证
仅访问您需要的部分——按地区、公司或用例划分。.
包含与领域专家的免费咨询,以帮助您做出决定。.
如需了解更多研究详情: 请申请免费样品
按服务分类:
聚焦服务领域,临床试验管理在全球临床试验支持服务市场中脱颖而出,占据了令人瞩目的54%的市场份额。临床试验管理涵盖一系列关键服务,包括患者招募、研究中心选择、数据管理、法规遵从和报告等。鉴于现代临床试验的复杂性,其方案涉及多个方面,患者群体多样化,且监管要求严格,因此,有效的管理至关重要。.
临床试验管理领域的蓬勃发展也可归因于临床试验日益全球化。由于研究往往在多个地点开展,甚至跨越多个国家或大洲,因此迫切需要集中管理,以确保研究的一致性和符合标准。这种对跨地域分散地点无缝、协调管理的需求,自然而然地促使企业加大对临床试验管理服务的投资和依赖。.
此外,随着行业向以患者为中心的模式和真实世界数据倾斜,临床试验管理的复杂性也随之增加,进一步凸显了该服务领域在全球临床试验支持服务市场中的重要性。确保患者依从性、整合真实世界数据以及利用数字化工具,如今已成为试验管理不可或缺的组成部分,这就需要专业的支持服务。.
区域分析
北美在临床试验支持服务市场中占据绝对领先地位,占据了令人瞩目的46.2%的市场份额。该地区的领先地位主要归功于美国,美国历来是突破性医学研究和创新的中心。北美拥有众多全球知名的研究机构和制药公司,临床研究领域也因此获得了大量资金投入。例如,仅在2021年,美国国立卫生研究院(NIH)就投入了超过410亿美元用于医学研究。如此强大的研究基础设施,加上美国食品药品监督管理局(FDA)严格的监管要求,使得临床试验需要种类繁多的专业支持服务,以确保其合规性、效率和质量。此外,精准医疗和基因疗法等新兴治疗领域的兴起,也使该地区的临床试验数量每年增长约8%,进一步推动了对支持服务的需求。.
另一方面,欧洲临床试验支持服务市场占据着举足轻重的地位,在临床试验支持服务领域占据超过26%的市场份额。欧洲多元化的人口结构和患者群体为其提供了独特的优势,尤其有利于那些旨在获得更具普遍性结果的临床试验。在2021-2022财年,德国、法国和英国等国在临床研究领域的总投资额高达150亿欧元,这表明该地区致力于推动医学进步。欧洲药品管理局(EMA)及其在成员国间持续推进监管协调的努力进一步增强了欧洲的吸引力。这些举措显著减少了该地区多国临床试验曾经面临的繁琐程序。因此,欧洲对临床试验支持服务的需求保持着约6%的年增长率。.
全球临床试验支持服务市场的主要参与者
- 查尔斯河实验室
- 科文斯公司.
- Icon PLC
- inVentiv国际制药服务
- IQVIA
- 美国实验室控股公司
- 诺沃泰克
- 帕雷塞尔国际
- 药品开发有限责任公司
- Quotient Bioresearch
- 药明康德
- 白血病和淋巴瘤协会(LLS)
- 其他主要球员
市场细分概述:
按试验类型
- 集中式临床试验
- 分散式临床试验
按治疗类型
- 小分子
- 生物制剂
- 医疗治疗类型
按阶段
- 临床前研究
- 第一阶段
- 第二阶段
- 第三阶段
- 第四阶段
按服务
- 网站管理
- 患者招募
- 临床试验管理
- 数据管理
- 其他的
通过申请
- 肿瘤学
- 中枢神经系统和精神障碍
- 心血管疾病
- 传染病
- 血液疾病
- 其他的
最终用户
- 制药和生物技术公司
- 合同研究组织(CRO)
- 医疗治疗类型公司
- 其他的
按地区
- 北美
- 美国
- 加拿大
- 墨西哥
- 欧洲
- 英国.
- 德国
- 法国
- 西班牙
- 波兰
- 比利时
- 芬兰
- 荷兰
- 葡萄牙
- 瑞典
- 瑞士
- 欧洲其他地区
- 亚太地区
- 中国
- 印度
- 日本
- 澳大利亚和新西兰
- 东盟
- 韩国
- 亚太其他地区
- 中东和非洲
- 阿联酋
- 沙特阿拉伯
- 卡塔尔
- 南非
- 摩洛哥
- 中东和非洲其他地区
- 南美洲
- 巴西
- 阿根廷
- 哥伦比亚
- 智利
- 秘鲁
- 南美洲其他地区
报告范围
| 报告属性 | 细节 |
|---|---|
| 2023年市场规模价值 | 252亿美元 |
| 预计2032年收入 | 471亿美元 |
| 历史数据 | 2019-2022 |
| 基准年 | 2023 |
| 预测期 | 2024-2032 |
| 单元 | 价值(十亿美元) |
| 复合年增长率 | 7.22% |
| 涵盖的领域 | 按试验类型、按治疗类型、按阶段、按服务、按应用、按最终用户、按地区 |
| 主要公司 | 查尔斯河实验室、科文斯公司、Icon PLC、inVentiv国际制药服务公司、IQVIA、美国实验室控股公司、诺沃泰克、Parexel国际、制药产品开发有限责任公司、Quotient Bioresearch、药明康德、白血病和淋巴瘤协会(LLS)以及其他主要参与者 |
| 定制范围 | 根据您的喜好获取定制报告。 欢迎提出定制需求 |
想要获取全面的市场信息?请联系我们的专家团队。.
与分析师交谈
.svg)