Japanischer Pharmamarkt: Nach Arzneimitteltyp (Markenmedikamente, Generika, rezeptfreie Arzneimittel); Darreichungsform (Tabletten, Kapseln, Injektionslösungen, Sprays, Suspensionen, Pulver, Sonstige Darreichungsformen); Verabreichungsweg (Oral, Topisch, Parenteral, Inhalation, Sonstige Verabreichungswege); Therapiegebiet (Herz-Kreislauf-Erkrankungen, Schmerzen, Krebs, Atemwegserkrankungen, Neurologische Erkrankungen, Orthopädie, Sonstige Therapiegebiete); Produktionsstätte (Eigenproduktion, Fremdproduktion); Vertriebskanal (Einzelhandel, Nicht-Einzelhandel, Online-Handel) – Marktgröße, Branchendynamik, Chancenanalyse und Prognose für 2025–2033
- Letzte Aktualisierung: 21. Oktober 2025 | | Bericht-ID: AA0923598
Marktübersicht
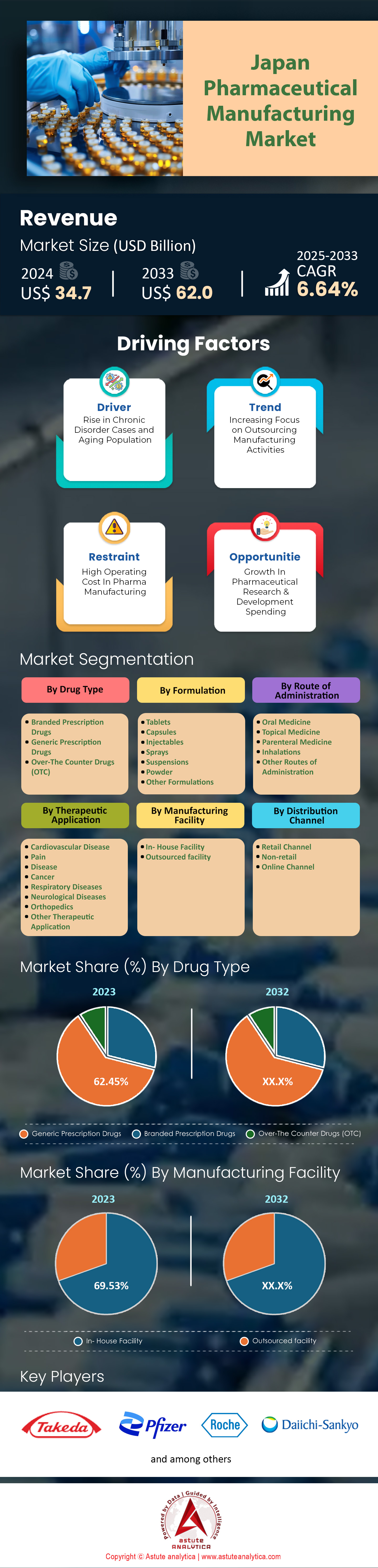
Der japanische Markt für die pharmazeutische Produktion wurde im Jahr 2024 auf 34,7 Milliarden US-Dollar geschätzt und soll bis 2033 ein Marktvolumen von 62,0 Milliarden US-Dollar erreichen, was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 6,64 % im Prognosezeitraum 2025–2033 entspricht.
Der japanische Pharmamarkt verzeichnet 2024 einen deutlichen Aufschwung bei inländischen und internationalen Investitionen, gestützt auf Japans solide regulatorische Rahmenbedingungen und seine nachweisliche Innovationskraft. Shionogi hat seine Produktionskapazität für Grippemedikamente durch die Inbetriebnahme zweier spezialisierter Produktionslinien in diesem Jahr erhöht, um der weltweit steigenden Nachfrage gerecht zu werden. Eisai erhielt die Zulassung für drei experimentelle Therapien gegen neurologische Erkrankungen, was die staatliche Förderung bahnbrechender Medikamente unterstreicht. Chugai führte eine innovative mRNA-basierte Therapie für seltene Autoimmunerkrankungen ein und markierte damit den Beginn der Entwicklung fortschrittlicher biologischer Formulierungen. Fujifilm Toyama Chemical brachte Anfang 2024 ein Gentherapieprodukt für erbliche Netzhauterkrankungen auf den Markt und weckte damit Hoffnungen auf fortschrittliche Präzisionsbehandlungen. Angesichts des verstärkten Fokus auf Gesundheitssicherheit gab das japanische Ministerium für Gesundheit, Arbeit und Soziales grünes Licht für fünf neue Produkte der regenerativen Medizin zur Behandlung chronischer Krankheiten. Der Sektor hat sich somit zu einem Anziehungspunkt für Spitzenforschung entwickelt und ein beispielloses Wachstum erlebt.
Zentral für diesen Aufschwung im pharmazeutischen Produktionsmarkt ist eine Kombination aus technologischer Zusammenarbeit, einem starken Patentumfeld und einer rasch alternden Bevölkerung. Takeda startete vier neue Onkologie-Studien mit monoklonalen Antikörpern der nächsten Generation und unterstrich damit den Fokus auf innovative Therapien. Kyowa Kirin meldete eine stabile Pipeline von fünf enzymbasierten Pharmakotherapien zur Behandlung seltener Stoffwechselerkrankungen und verdeutlichte damit den Fokus des Landes auf spezialisierte Medizin. Mitsubishi Tanabe ergriff 2024 Maßnahmen zum Aufbau zweier hochmoderner Produktionsstätten in Osaka und Kobe, um die lokale Herstellung von Biosimilars zu ermöglichen. Otsuka eröffnete in Tokio ein spezialisiertes Forschungszentrum mit sechs Gen-Editing-Laboren und unterstrich damit das Bestreben nach genomischen Durchbrüchen. Die Nachfrage nach innovativen Herstellungsverfahren führte zu einer Welle von Joint Ventures und einem Anstieg kleinerer Biotech-Unternehmen, die fortschrittliche Forschungsinstrumente liefern. Diese Synergie zwischen etablierten Unternehmen und aufstrebenden Startups hat die Produktionszeiten deutlich verkürzt und die Erwartungen an ein nachhaltiges Marktwachstum erhöht.
Unter den verschiedenen Arzneimitteltypen besteht eine konstante Nachfrage nach niedermolekularen Formulierungen, doch die eigentliche Dynamik geht von Immuntherapien, zellbasierten Produkten und fortschrittlichen Biologika aus. Daiichi Sankyo hat kürzlich drei Produktionslinien für Antikörper-Wirkstoff-Konjugate im pharmazeutischen Fertigungsmarkt fertiggestellt und damit den Trend zu gezielteren Therapien und spezialisierten Formulierungen unterstrichen. Allein im Jahr 2024 kooperierte RIKEN mit drei lokalen Herstellern, um Zellvermehrungstechnologien für Krebsimmuntherapien weiterzuentwickeln und verdeutlichte so die Synergie zwischen Forschungsinstituten und Industrie. Beliebte therapeutische Anwendungen konzentrieren sich auf Onkologie, Neurologie und Herz-Kreislauf-Erkrankungen, die jeweils von beschleunigten Zulassungsverfahren und spezialisierten Forschungszentren in den großen Städten profitieren. Die gemeinsamen Anstrengungen von Pharmariesen und Forschungsinstituten erweitern die Grenzen der Präzisionsmedizin und ermöglichen es Japan, an der Spitze der globalen Gesundheitsinnovation zu bleiben. Mit dem Ausbau der nationalen Infrastruktur wächst auch die Nachfrage des Inlandsmarktes nach modernen Therapien und festigt Japans Position als wichtiger Akteur in der globalen Pharmalandschaft.
Für weitere Einblicke fordern Sie ein kostenloses Muster an.
Marktdynamik
Treiber: Verstärkte klinische Kooperationen treiben die Entwicklung innovativer Biologika in nationalen und internationalen Produktionsnetzwerken voran
Kooperative Forschungs- und Entwicklungsansätze entwickeln sich zu einem zentralen Treiber im japanischen Pharmamarkt. Viele Unternehmen legen verstärkt Wert auf gebündeltes Fachwissen und einen reibungslosen Übergang von Laborergebnissen zur skalierbaren Produktion. Diese Allianzen werden durch ein politisches Umfeld gefördert, das klinische Studien in frühen Phasen und die Zusammenarbeit verschiedener Institutionen unterstützt. So können Unternehmen spezialisiertes Wissen nutzen und gleichzeitig die Risiken komplexer Biologika-Projekte streuen. Die Hinwendung zu gemeinsamen Protokollen hat den Bedarf an innovativen Therapien in den Bereichen Onkologie, Immunologie und regenerative Medizin verstärkt. Anfang 2024 stellte Otsuka in Zusammenarbeit mit einem internationalen klinischen Konsortium ein neu entwickeltes Forschungsprogramm für monoklonale Antikörper vor und unterstrich damit die Bedeutung globaler Expertise für die Entwicklung von Therapien der nächsten Generation. Ein Biotech-Unternehmen aus Kobe sicherte sich staatliche Förderung für eine experimentelle zellbasierte Therapie gegen akute neurologische Erkrankungen. Dies deutet darauf hin, dass die Zusammenarbeit zwischen öffentlichem und privatem Sektor zu einem wichtigen Katalysator für Pionierarbeit wird.
Gemeinsame Initiativen tragen auch zur Optimierung von Herstellungsprozessen im pharmazeutischen Markt bei und gewährleisten, dass vielversprechende Produktinnovationen zeitnah in marktreife Produkte umgesetzt werden können. Die gegenseitige Nutzung standardisierter Datensysteme und synchronisierter Studienphasen reduziert Doppelarbeit und beschleunigt die Zulassungsverfahren – ein entscheidender Vorteil im sich rasant entwickelnden Bereich der Biologika. Viele Partnerschaften reichen über nationale Grenzen hinaus und konzentrieren sich auf den Wissensaustausch zu fortschrittlichen Herstellungsverfahren wie kontinuierlicher Verarbeitung und Echtzeitanalyse. Im Februar 2024 kündigte Takeda eine Zusammenarbeit mit Biological E. Limited (BE) zur Steigerung der Produktion seines Dengue-Impfstoffs QDENGA an. Ziel dieser Partnerschaft ist es, die Produktionskapazität auf 50 Millionen Dosen jährlich zu erhöhen, was Takedas Ziel, bis spätestens 2030 jährlich 100 Millionen Dosen bereitzustellen, maßgeblich unterstützen wird. Diese Initiative ist Teil von Takedas umfassenderer Strategie, den Zugang zum Impfstoff in Regionen mit endemischer Dengue-Fieber-Verbreitung zu verbessern. Shionogi beteiligte sich an einem gemeinsamen Netzwerk für klinische Studien zur Bewertung biologischer Kandidaten für seltene Erkrankungen und verdeutlichte damit die zunehmende Bedeutung internationaler Kooperationen. Chugai strebte nach schnelleren Markteinführungswegen und initiierte daher in Zusammenarbeit mit einem Universitätsklinikum eine Pilotstudie, um die Zeitspanne zwischen Pilotproduktion und kommerzieller Distribution zu verkürzen. Durch die Stärkung dieser vielseitigen Kooperationen sind japanische Pharmaunternehmen bestens gerüstet, um innovative Lösungen für Bereiche mit hohem ungedecktem medizinischem Bedarf zu entwickeln und Japan damit an die Spitze modernster Biologika-Therapien zu bringen.
Trend: Zunehmender Einsatz von intelligenter Robotik und automatisierten Anlagen verbessert die Arzneimittelqualität und -konsistenz weiter
Ein deutlicher Trend hin zu Robotik und automatisierten Plattformen verändert die operativen Kernprozesse der japanischen Pharmaindustrie. Unternehmen modernisieren ihre Anlagen rasant, um unbemannte Prozesse und kontinuierliche Produktion zu ermöglichen, und investieren erhebliche Ressourcen in digitale Technologien, die höhere Konsistenz und schnelleren Durchsatz versprechen. Diese Entwicklung spiegelt den marktweiten Trend wider, menschliche Eingriffe in Bereichen wie steriler Abfüllung, Mischen und Wirkstoffhandhabung zu minimieren und so eine höhere Präzision für fortschrittliche Therapeutika wie Biologika und zellbasierte Behandlungen zu gewährleisten. Viele Unternehmen setzen Roboter auch für repetitive Aufgaben ein, die die strikte Einhaltung kontaminationsfreier Bedingungen erfordern. Anfang 2024 integrierte eine hochmoderne Anlage in Nagoya Robotersysteme für die Handhabung hochwirksamer Wirkstoffe und unterstrich damit die wachsende Bedeutung vollständig geschlossener Produktionszyklen. Fujifilm Toyama Chemical implementierte ein KI-gestütztes Steuerungssystem zur Echtzeitüberwachung der Molekülstabilität und verdeutlichte damit die Rolle prädiktiver Analysen in der modernen Fertigung.
Automatisierungsstrategien optimieren nicht nur Routineaufgaben, sondern bilden auch die Brücke zu fortschrittlicher Qualitätssicherung. Die Echtzeit-Datenerfassung in jeder Produktionsphase ermöglicht die sofortige Anpassung von Temperatur, Druck oder Mischparametern – ein entscheidender Faktor bei der Handhabung empfindlicher Biologika. KI-Systeme in der pharmazeutischen Produktion helfen, Fehler vorherzusagen und liefern so wertvolles Feedback für Forschungs- und Entwicklungsteams. 2024 nahm eine weitere automatisierte Produktionslinie in Shizuoka den Einsatz von Bildverarbeitung zur Erkennung kleinster Abweichungen in Tablettenbeschichtungen in Betrieb – ein Schritt, der die hohen Anforderungen an präzise Dosierung widerspiegelt. Chugai testete robotergestützte Probenahmesysteme für genbasierte Formulierungen, um die bisher stark manuell geprägten Probenahmeprotokolle zu optimieren. Ein Pilotprojekt mit einem japanischen Technologie-Startup führte eine automatisierte Desinfektionseinheit für Zellkulturräume ein und setzte neue Maßstäbe in der Kontaminationskontrolle. Mit zunehmender Komplexität von Robotik und Automatisierung gewinnt Japans Pharmasektor einen entscheidenden Wettbewerbsvorteil bei der Bereitstellung sicherer und konsistenter Therapien. Dies verdeutlicht, wie moderne Technologie die Qualität der Arzneimittelherstellung grundlegend verbessern kann.
Herausforderung: Rasante und komplexe Verschiebung der F&E-Prioritäten führt zu Ungleichgewichten in den optimierten klinischen und kommerziellen Produktionsabläufen
Trotz bedeutender Fortschritte im japanischen Pharmamarkt stellen die ständigen Neuausrichtungen der Forschungsprioritäten eine konkrete Herausforderung für Unternehmen dar, die eine effiziente Produktion aufrechterhalten wollen. Firmen passen ihre Produktpipelines häufig an neue Entdeckungen an, wie beispielsweise Durchbrüche in der Genomeditierung oder neu entdeckte biologische Signalwege. Dadurch gerät die bestehende Infrastruktur mit den aktualisierten klinischen Zielen in Konflikt. Diese Diskrepanz kann zu ungenutzten Anlagen, Schulungsbedarf für Mitarbeiter und verlängerten Produktionszeiten führen, da die Produktionsstätten sich anpassen müssen. Die veränderten Schwerpunkte erschweren auch das Lieferkettenmanagement; Reagenzien und Spezialmaterialien, die für bestimmte Wirkstoffgruppen vorgesehen sind, können überflüssig werden, wenn sich strategische Interessen plötzlich ändern. Ein Biotech-Unternehmen aus Osaka stellte kürzlich die Entwicklung eines Antibiotikums in der Spätphase ein, um sich auf fortgeschrittene Immuntherapien zu konzentrieren. Dies verdeutlicht, wie abrupte Neuausrichtungen etablierte Arbeitsabläufe stören können. Anfang 2024 nutzte eine Forschungsabteilung eines großen Pharmaunternehmens in Tokio eine einzelne High-End-Produktionsanlage, die für ein eingestelltes Neurologieprojekt vorgesehen war, um. Dies zeigt die weitreichenden Folgen plötzlicher Umstrukturierungen der Produktpipeline.
Solche Ungleichgewichte verstärken sich in Bereichen, die Präzisionstechnik erfordern, wo funktionsübergreifende Kompatibilität für einen reibungslosen Übergang von der Pilot- zur Produktionsphase entscheidend ist. Schnelle Veränderungen im Therapieschwerpunkt erfordern eine zügige Revalidierung von Prozessen, Protokollen und Automatisierungssteuerungen auf dem japanischen Pharmamarkt. Diese Belastung betrifft auch die Compliance-Teams, die neue behördliche Zulassungen einholen oder bestehende Anträge für aktualisierte Anwendungsgebiete anpassen müssen. Mitte 2024 überarbeitete Takeda einen zuvor zugelassenen Herstellungsprozess für Biologika, um Änderungen in den Formulierungstechniken zu berücksichtigen, was zu einer ungeplanten dreimonatigen Verzögerung führte, bevor das Unternehmen die Produktion wieder aufnehmen konnte. Eine weitere Herausforderung entsteht, wenn Mitarbeiter mit Spezialkenntnissen auf völlig andere Anwendungen umsteigen müssen. Ein spezialisiertes Immunologie-Team in Yokohama wurde einem neuen RNA-basierten Projekt zugeteilt, was das Unternehmen zu Investitionen in Umschulungen zwang. Ein gemeinsamer Studienstandort in Kyoto musste aufgrund einer unerwarteten Umstrukturierung der Pipeline im Bereich Neurologie ebenfalls kurzzeitig stillgelegt werden. Diese sich überschneidenden Anpassungen verdeutlichen die Komplexität des Managements zukunftsweisender Pipelines und unterstreichen die Notwendigkeit vorausschauender Strategien, die wissenschaftliche Forschung mit stabiler und konsistenter Produktionskapazität in Einklang bringen.
Segmentanalyse
Nach Arzneimitteltyp: Generika führen mit einem Marktanteil von über 28,19 %
Generische verschreibungspflichtige Medikamente haben sich auf dem japanischen Pharmamarkt aufgrund einer Kombination aus politischer Förderung, strengen Qualitätskontrollen und dem Fokus auf bezahlbare Gesundheitsversorgung stark etabliert. Staatliche Anreize, insbesondere vom Ministerium für Gesundheit, Arbeit und Soziales, ermutigen Ärzte, bioäquivalente Alternativen zu verschreiben. Auch das gestiegene Bewusstsein der Verbraucher trägt zu dieser Präferenz bei, da Patienten mit chronischen Erkrankungen wissen, dass Generika die gleichen Wirkstoffe wie die Originalpräparate enthalten. Sawai Pharmaceutical beispielsweise berichtete, im Jahr 2023 über 2.700 verschiedene Generika entwickelt zu haben – von Herz-Kreislauf-Medikamenten bis hin zu entzündungshemmenden Mitteln – was die Breite des Angebots unterstreicht. Laut einer Studie des Japanischen Generika-Verbandes vom März 2023 werden landesweit schätzungsweise 5,6 Millionen Rezepte für Generika pro Tag eingelöst. Ein weiterer Faktor ist die wachsende Kostendifferenz bei Antibiotika-Therapien: Eine Standardbehandlung mit dem Markenmedikament Augmentin kostet etwa 2.300 Yen, während das entsprechende Generikum nur 800 Yen kostet.
Parallel zur Erschwinglichkeit haben große Produktionskapazitäten die breite Akzeptanz von Generika auf dem pharmazeutischen Markt vorangetrieben. Allein im ersten Halbjahr 2023 produzierte Towa Pharmaceutical über 800 Millionen Einheiten blutdrucksenkender Generika und demonstrierte damit die industrielle Stärke hinter der Generika-Expansion. Nichi-Iko hat seine Position durch die Bereitstellung von 14 Milliarden Yen für Forschung und Entwicklung in diesem Jahr gestärkt, wobei ein Großteil davon in die Entwicklung qualitätsgesicherter, bioäquivalenter Arzneimittel fließt. Die Richtlinien des Ministeriums für 2023 legen Generika zudem in mindestens 22 wichtigen Therapiebereichen als Standard fest und spiegeln damit ein regulatorisches Umfeld wider, das kosteneffiziente Lösungen ohne Kompromisse bei der Sicherheit fördert. Diese Maßnahmen entlasten die alternde Bevölkerung Japans, deren Medikamente oft über einen längeren Zeitraum eingenommen werden müssen. Durch die Abstimmung von Patientenbedürfnissen, Regierungspolitik und leistungsstarker Produktionsinfrastruktur haben sich Generika einen zentralen Platz in der japanischen Pharmalandschaft gesichert und zeigen beispielhaft, wie Kosten- und Qualitätsüberlegungen harmonisch zur Marktführerschaft beitragen können.
Nach Darreichungsform: Tabletten dominieren mit über 32 % den japanischen Pharmamarkt
Tabletten spielen in Japan eine bedeutende Rolle bei pharmazeutischen Darreichungsformen, vor allem aufgrund ihrer einfachen Dosierung, Stabilität und unkomplizierten Massenproduktion. Patienten schätzen insbesondere in der Geriatrie die leichte Schluckbarkeit und die Möglichkeit, Tabletten zu teilen oder zu zerkleinern. Ein prominentes Beispiel ist die 2023 von Eisai eingeführte Schmelztablette für Alzheimer-Patienten, die sich sofort auflöst und von Krankenhäusern für Demenzstationen auf Vorrat gekauft wurde. Dieser Fokus auf patientenfreundliches Design unterstreicht, warum viele Forschungsteams an der Optimierung von Tablettenbeschichtungen für eine geschmacksneutrale Einnahme arbeiten. Laut einer Veröffentlichung der Japanischen Gesellschaft für Pharmazeutische Technologie aus dem Jahr 2023 sind in japanischen Fabriken rund 1.200 spezialisierte Produktionslinien für die Tablettenpressung und Filmbeschichtung vorgesehen. KYORIN Pharmaceutical investierte im vergangenen Jahr rund 6 Milliarden Yen in hochmoderne Tablettenpressen, um die Produktionseffizienz zu steigern.
Die Bevorzugung von Tabletten gegenüber Kapseln, Injektionspräparaten und anderen Darreichungsformen beruht auch auf den Vorteilen hinsichtlich Haltbarkeit und Vertriebsflexibilität im pharmazeutischen Markt. Viele Generika, von Mitteln gegen Magengeschwüre bis hin zu Antihistaminika, werden je nach Dosierungsbedarf als Tabletten mit schneller oder verzögerter Wirkstofffreisetzung angeboten. Tabletten eignen sich besonders gut für innovative Verpackungen, wie beispielsweise die Einführung kindersicherer Blisterverpackungen durch Takeda Pharmaceutical im Jahr 2023 für mehr Sicherheit im Haushalt zeigt. Auch Krankenhäuser und Apotheken schätzen die Vorteile von Tabletten für die vereinfachte Lagerverwaltung. Der Großhändler Suzuken bestätigte in diesem Jahr Lieferungen von mindestens 350.000 Tablettenpackungen pro Tag in großen Ballungszentren. Darüber hinaus spielt die Synergie in der Produktion eine Rolle: Eine einzige Produktionslinie kann oft mit minimalen Ausfallzeiten zwischen verschiedenen Arten von Tablettenpräparaten wechseln. Diese Anpassungsfähigkeit senkt die Betriebskosten und sichert eine kontinuierliche Versorgung, wodurch die führende Rolle von Tabletten in der japanischen Pharmaindustrie weiter gestärkt wird.
Nach therapeutischen Anwendungsgebieten: Über 33 % der hergestellten Arzneimittel werden zur Schmerzbehandlung eingesetzt
Japans Fokus auf die Herstellung von Schmerzmitteln ist auf die sich verändernde Patientendemografie und die sich wandelnden klinischen Behandlungsmuster zurückzuführen. Laut Angaben der Japanischen Gesellschaft für Schmerzforschung (Japanese Association for the Study of Pain, 2023) leiden über 23 Millionen Menschen an chronischen Schmerzen, die auf Erkrankungen des Bewegungsapparates, Neuropathien oder den Alterungsprozess zurückzuführen sind. Ibuprofen-Tabletten zählen neben Paracetamol und Naproxen zu den am häufigsten produzierten Schmerzmitteln auf dem pharmazeutischen Markt. Daiichi Sankyo meldete im ersten Quartal 2023 eine Produktion von fast 450 Millionen Ibuprofen-Tabletten. Die zunehmende Verbreitung von Arthrose und rheumatoider Arthritis in der alternden Bevölkerung hat die Nachfrage nach modernen nichtsteroidalen Antirheumatika (NSAR) weiter angekurbelt. Die Japanische Gesellschaft für Primärversorgung (Japan Primary Care Association) gibt an, dass akute Schmerzen infolge von Verletzungen und medizinischen Eingriffen jährlich etwa 5 Millionen Patienten betreffen, was die verstärkte Nutzung von Opioid- und Nicht-Opioid-Schmerzmitteln erklärt.
Pharmaunternehmen haben ihr Angebot um Kombinationspräparate und neuartige Formulierungen zur Schmerztherapie erweitert. Takedas Tramadol mit verlängerter Wirkstofffreisetzung, das dieses Jahr auf den Markt kam, ist für chronische Rückenschmerzen geeignet und wird monatlich rund 1,2 Millionen Mal verschrieben. Teijin Pharma, einer der wichtigsten Akteure im japanischen Pharmamarkt, hat als Pionier transdermale Pflaster mit Buprenorphin für Patienten mit Schluckbeschwerden entwickelt und ermöglicht so eine gezieltere und nachhaltigere Schmerzkontrolle. Innovative Studien des Nationalen Zentrums für Geriatrie und Gerontologie aus dem Jahr 2023 unterstreichen die Bedeutung multimodaler Therapien, die Physiotherapie integrieren; Medikamente bleiben jedoch ein Eckpfeiler. Dank Investitionen von Organisationen wie der Japanischen Agentur für Medizinische Forschung und Entwicklung (JAMRD) konzentrieren japanische Unternehmen ihre Ressourcen auf die Verbesserung der schmerzstillenden Wirkung bei gleichzeitiger Reduzierung von Nebenwirkungen. Diese gemeinsamen Anstrengungen spiegeln ein Gesundheitssystem wider, das Schmerz als vielschichtiges Problem anerkennt und so die starke japanische Produktion von Schmerzmitteln fördert.
Nach Produktionsstätte: Eigene Produktionsstätten glänzen im japanischen Pharmamarkt und kontrollieren einen Marktanteil von über 69,5 %
Japans Vorliebe für die Eigenproduktion von Arzneimitteln wurzelt tief in strengen Qualitätsstandards, dem Schutz geistigen Eigentums und dem Stolz der Unternehmen auf ihre lokale Fertigung. Bedeutende japanische Akteure wie Astellas Pharma, Takeda Pharmaceutical und Otsuka Holdings unterhalten umfangreiche eigene Produktionsanlagen und unterstreichen damit eine Strategie, die die direkte Kontrolle der Lieferkette priorisiert. Laut einem Branchenbericht des japanischen Pharmaherstellerverbands aus dem Jahr 2023 arbeiten rund 1.500 Hochsicherheitsanlagen nach den Richtlinien der Guten Herstellungspraxis (GMP), um Biosicherheit und höchste Wirksamkeit zu gewährleisten. Durch die Zusammenlegung von Forschung, Formulierung und Verpackung unter einem Dach können diese Unternehmen schnell auf regulatorische Änderungen und Marktbedürfnisse reagieren, ohne die Komplexität globaler Auslagerung in Kauf nehmen zu müssen. Mitsubishi Tanabe Pharma investierte dieses Jahr 22 Milliarden Yen in die Modernisierung seiner Anlagen, die mit fortschrittlicher Automatisierung für die sterile Herstellung ausgestattet sind.
Die Eigenproduktion ist auch auf den kulturellen Fokus auf Vertrauen und Rückverfolgbarkeit im pharmazeutischen Herstellungsmarkt zurückzuführen. Die Japan Health Sciences Foundation stellte in einem Briefing von 2023 fest, dass das Vertrauen der Patienten steigt, wenn Produkte ein bekanntes inländisches Etikett tragen, insbesondere in sensiblen Bereichen wie Onkologie oder Biologika. Skandale um minderwertige Importe in den vergangenen Jahrzehnten bestärkten das nationale Engagement für strengere Kontrollen im Inland. Der integrierte Forschungs- und Produktionscampus von Shionogi & Co. in Osaka ist ein Beispiel für dieses Modell und vereint Wirkstoffforschung, Pilotproduktion und kommerzielle Skalierung unter einem Dach. Mit dem Ausbau der lokalen Kapazitäten wächst auch die Technologieakzeptanz: Robotik für die Tablettenprüfung, intelligente Sensoren für die kontinuierliche Fertigung und datengetriebene Analysen zur Prozessoptimierung. Indem sie diese Prozesse im eigenen Haus durchführen, sichern japanische Pharmariesen eine gleichbleibende Qualität und schützen gleichzeitig firmeneigene Forschungsergebnisse. Dadurch wird die inländische Produktion zu einer strategischen Säule des japanischen Pharmasektors.
Diesen Bericht anpassen + von einem Experten validieren
Greifen Sie nur auf die Abschnitte zu, die Sie benötigen – regionsspezifisch, unternehmensbezogen oder nach Anwendungsfall.
Beinhaltet eine kostenlose Beratung mit einem Domain-Experten, der Sie bei Ihrer Entscheidung unterstützt.
Um mehr über diese Studie zu erfahren: Fordern Sie ein kostenloses Muster an
Führende Akteure auf dem japanischen Markt für pharmazeutische Herstellung
- Abbott Laboratories
- AbbVie Inc.
- ACADIA Pharma
- Aenova-Gruppe
- Amgen
- Astellas Pharma Inc.
- AstraZeneca
- Bayer AG
- Biogen
- Boehringer Ingelheim International GmbH
- Chugai Pharmaceutical Co., Ltd
- Daiichi Sankyo
- Eli Lilly and Company
- F. Hoffmann-La Roche Ltd.
- GlaxoSmithKline plc
- Johnson & Johnson
- Merck & Co., Inc.
- Novartis AG
- Novo Nordisk
- Pfizer, Inc.
- Sanofi SA
- Takeda
- Weitere prominente Spieler
Marktsegmentierungsübersicht:
Nach Arzneimitteltyp
- Markenmedikamente auf Rezept
- Generische verschreibungspflichtige Medikamente
- Rezeptfreie Arzneimittel (OTC)
Durch Formulierung
- Tabletten
- Kapseln
- Injektionspräparate
- Sprays
- Federungen
- Pulver
- Andere Formulierungen
Auf dem Weg der Verwaltung
- Orale Medizin
- Topische Medizin
- Parenterale Medizin
- Inhalationen
- Andere Verabreichungswege
Durch therapeutische Anwendung
- Herz-Kreislauf-Erkrankungen
- Schmerz
- Krankheit
- Krebs
- Atemwegserkrankungen
- Neurologische Erkrankungen
- Orthopädie
- Weitere therapeutische Anwendungen
Nach Produktionsstätte
- Eigene Einrichtung
- Ausgelagerte Einrichtung
Nach Vertriebskanal
- Einzelhandelskanal
- Nicht-Einzelhandel
- Online-Kanal
BERICHTSUMFANG
| Berichtattribute | Details |
|---|---|
| Marktgröße im Jahr 2024 | 34,7 Milliarden US-Dollar |
| Erwartete Einnahmen im Jahr 2033 | 62,0 Milliarden US-Dollar |
| Historische Daten | 2020-2023 |
| Basisjahr | 2024 |
| Prognosezeitraum | 2025-2033 |
| Einheit | Wert (Mrd. USD) |
| CAGR | 6.64% |
| Abgedeckte Segmente | Nach Arzneimitteltyp, Darreichungsform, Verabreichungsweg, therapeutischer Anwendung, Herstellungsstätte, Vertriebskanal |
| Wichtige Unternehmen | Abbott Laboratories, AbbVie Inc., ACADIA Pharma, Aenova Group, Amgen, Astellas Pharma Inc., AstraZeneca, Bayer AG, Biogen, Boehringer Ingelheim, Ingelheim International GmbH, Chugai Pharmaceutical Co., Ltd., Daiichi Sankyo, Eli Lilly and Company, F. Hoffmann-La Roche Ltd., GlaxoSmithKline plc, Johnson & Johnson, Merck & Co., Inc., Novartis AG, Novo Nordisk, Pfizer, Inc., Sanofi SA, Takeda und weitere bedeutende Akteure |
| Anpassungsumfang | Erhalten Sie Ihren individuell angepassten Bericht nach Ihren Wünschen. Fragen Sie nach individuellen Anpassungen. |
SIE SUCHEN UMFASSENDES MARKTWISSEN? KONTAKTIEREN SIE UNSERE EXPERTEN.
SPRECHEN SIE MIT EINEM ANALYSTEN
.svg)