世界の臨床試験支援サービス市場:試験タイプ別(集中型臨床試験および分散型臨床試験)、治療タイプ別(低分子、生物学的製剤、医療治療タイプ)、フェーズ別(前臨床試験、フェーズI、フェーズII、フェーズIII、フェーズIV)、サービス別(サイト管理、患者募集、臨床試験管理、データ管理、その他)、アプリケーション別(腫瘍学、中枢神経系および精神疾患、心血管疾患、感染症、血液疾患、その他)、エンドユーザー別(製薬およびバイオテクノロジー企業、開発業務受託機関(CRO)、医療治療タイプ企業、その他)、地域別市場規模、業界動向、機会分析、および2024~2032年の予測
- 最終更新日: 2024年2月26日 | | レポートID: AA0923622
市場シナリオ
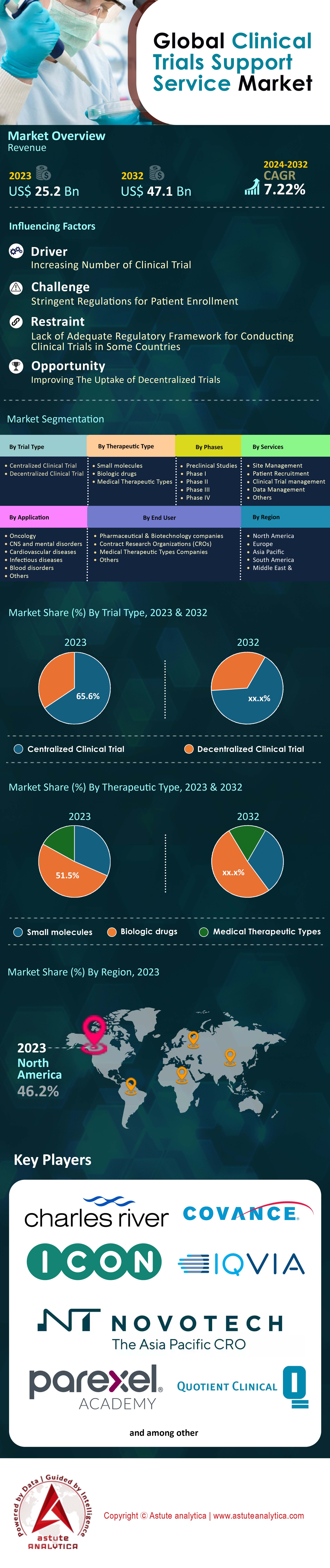
世界の 臨床試験支援サービス市場は と評価され 、2023年に252億米ドル 成長し、 2032年には471億米ドルを で 平均成長率(CAGR)7.22% の予測期間中に年 。
臨床試験支援サービス市場は、世界のヘルスケア業界にとって不可欠な基盤であり、革新的な治療法や画期的な治療薬の創出において極めて重要な役割を果たしています。世界中で様々な疾患や病状の急増が見られる中、より新しく、より安全で、より効果的な治療法の開発がますます重要視されています。こうした動きにより、堅牢かつ合理化された臨床試験支援サービスの需要が大幅に高まっています。CDC(米国疾病対策センター)は最近の出版物で、特に感染症分野における臨床試験の急増を強調しています。この急増は、急速な研究とソリューション開発を必要とした近年の世界的な健康課題に起因すると考えられます。医薬品開発だけでなく、疾患の長期的な影響や合併症の可能性を理解することにも焦点が当てられており、これが長期的な臨床試験支援の需要をさらに高めています。.
米国における医薬品承認と臨床試験を管轄するもう一つの重要な機関であるFDAは、過去1年間で新薬承認申請(NDA)件数が15%増加したと報告した。この増加は、 製薬業界、臨床試験支援サービスの必要性の高まりも浮き彫りにしている。新薬や治療法の申請ごとに、膨大な量のデータを処理、管理、分析する必要があるため、こうした支援サービスの役割は不可欠となる。
臨床試験支援サービス市場における注目すべきトレンドは、患者中心の試験への移行です。FDAは患者報告アウトカムの重要性を強調しており、これが試験の複雑さをさらに増しています。患者の募集、維持、そしてリアルワールドデータの収集を支援するサービスが注目を集めています。この進化により、専門的な支援サービスへの需要が急増し、市場をさらに推進しています。地域別に見ると、北米、特に米国は依然として臨床試験市場において重要なプレーヤーです。しかし、中国やインドなどの国々が主導するアジア太平洋地域は、臨床研究の拠点として急速に台頭しています。この変化は、熟練した労働力、高度なインフラ、そして好ましい規制環境の組み合わせによって推進されています。最新のレポートによると、アジア太平洋地域の臨床試験は9%の成長率を記録し、世界平均を上回っています。.
さらに詳しい情報を得るには、 無料サンプルをリクエストしてください。
市場動向
推進力:データ分析と人工知能における技術の進歩
高度なデータ分析と人工知能(AI)の統合は、臨床試験支援サービス市場を牽引する重要な原動力となっています。歴史的に、臨床試験は手作業が中心でしたが、現在では技術が大きく進歩しています。例えば、2022年には、1つの第III相臨床試験で3テラバイト以上のデータが生成されると推定されています。2025年までにデータ生成量は年間10%増加すると予測されており、その膨大な量は膨大なものとなっています。.
急増するデータに対処するため、AIと高度な分析を活用したツールが変革をもたらしています。2025年までに、臨床試験支援サービスの65%以上がAIまたは同様の高度な分析を業務に導入すると予想されています。これは単なる技術的なメリットではなく、財務的な影響ももたらします。医薬品開発プロセスにAIツールを導入することで、15~20%のコスト削減が見込まれます。2021年、臨床試験支援サービスによる市場承認を得た新薬の開発コストが平均で約26億ドルであったことを考えると、AIによるコスト削減の可能性は数十億ドルに上ります。.
さらに、AIを活用した予測分析は、医薬品開発における意思決定のダイナミクスを変革しました。以前は、薬物経路の実現可能性を判断するのに数ヶ月かかっていました。しかし、AIの登場により、そのような判断は数週間、時には数日で行われるようになりました。ある調査では、AIを活用している製薬会社の約70%が、意思決定の期間を半分に短縮できたことが示されています。.
トレンド:臨床試験における患者の多様性の重視
臨床試験支援サービス市場で勢いを増している顕著なトレンドは、患者の多様性への重視の高まりです。数年前までは、臨床試験における多様性は主要な焦点ではありませんでした。しかし、2019年には、多様な患者基盤を持つと報告された臨床試験は約20%にとどまりました。2022年までに、この数字は35%に急増しました。この傾向は、2025年までに新規臨床試験の半数以上が患者の多様性を優先するようになることを示唆しています。規制当局はこのトレンドに大きな影響を与えています。例えば、FDAが2020年に臨床試験における患者の多様性の必要性を強調するガイドラインを発表した際、業界に大きな波紋が広がりました。これらのガイドラインの発表後、製薬会社の約40%が、より幅広く多様な参加者基盤を確保するために、募集戦略を見直したと報告しています。.
臨床試験における多様性は、代表性の問題だけでなく、経済的にも健全な戦略です。より多様な患者層で試験された医薬品は、規制当局の承認プロセスにおけるハードルが低くなる可能性が高く、臨床試験支援サービス市場への市場参入が迅速化されます。試算によると、多様な試験を重視する企業は、医薬品の市場投入までの時間を最大6か月短縮できるとされています。これは、収益を10~15%増加させる可能性があります。さらに、多様性に重点を置くことは、信頼の構築という、目に見えないながらも大きな効果をもたらします。歴史的に、代表性の低いコミュニティは、臨床研究に対して懐疑的であることが多くありました。しかし、2022年の調査では、これらのコミュニティの回答者の60%が、臨床試験が多様性を重視していることを知っていれば、より積極的に参加するだろうことが明らかになりました。.
課題:臨床試験におけるデータのプライバシーとセキュリティに関する懸念
世界の臨床試験支援サービス市場において、データのプライバシーとセキュリティの確保という大きな課題が存在します。臨床試験がデジタルプラットフォームへの移行を進めるにつれ、生成される膨大な量の機密性の高い患者データは、情報漏洩や不正アクセスのリスクが高まっています。電子カルテやデジタルデータ収集ツールへの移行は、効率性を高める一方で、システムの脆弱性を増大させています。例えば、2021年には、医療データを標的としたサイバー攻撃が前年比で30%増加したと報告されています。こうした攻撃は、試験の完全性を脅かすだけでなく、被験者のプライバシーを危険にさらし、個人の健康情報を漏洩させる可能性があります。.
多くの臨床試験がグローバルに行われるという性質上、複雑さが増しています。各国にはデータプライバシーに関する独自の規制や基準があり、製薬会社や臨床試験主催者にとって、こうした多様な規制環境への対応は困難な場合があります。2022年の調査では、国際臨床試験の約40%が、各国間のデータプライバシー基準の相違により規制上の障害に直面していることが明らかになりました。こうした課題の影響は多岐にわたります。臨床試験への患者参加の礎となる信頼が危機に瀕しています。参加者が自分のデータが危険にさらされていると感じると、参加する可能性が低くなり、命を救う可能性のある研究の進展を妨げる可能性があります。デジタル変革が進む時代において、堅牢なデータプライバシーとセキュリティを確保することは、世界の臨床試験支援サービス市場にとって依然として重要な課題です。.
セグメント分析
トライアルタイプ別:
試験の種類別に見ると、集中型臨床試験セグメントは、世界の臨床試験支援サービス市場において際立った存在となっています。市場シェアの65.6%を占め、明確な優位性を確立しています。歴史的に見ても、集中型臨床試験は研究分野において常に重要な役割を果たしており、標準化されたプロトコル、統一されたデータ収集方法、そして合理化されたコミュニケーションチャネルといった利点を提供しています。.
で最も速い成長が見込まれています 率(CAGR)7.41。これらの予測が実現すれば、同分野の市場シェアは今世紀末までに70%に近づき、そのリーダーシップをさらに確固たるものにするでしょう。この成長加速の要因としては、試験の複雑化、複数地域で行われる臨床試験の増加、そして集中型試験がコスト効率と時間効率の面でもたらすメリットが挙げられます。
治療の種類別:
治療面では、市場はバイオ医薬品への明確な傾きを示しています。市場シェアの51.5%という高いシェアを占めるバイオ医薬品は、世界の臨床試験支援サービス市場において主力となっています。バイオ医薬品は、その複雑な性質と、自己免疫疾患からがんまで幅広い疾患の治療への可能性から、研究への関心と投資が急増しています。.
さらに、この傾向は当面停滞する兆しは見られません。集中型臨床試験セグメントに見られる成長パターンを反映して、生物製剤は 7.41%という最も高い年平均成長率(CAGR) 。生物製剤セグメントのこの着実な成長は、数多くの要因によって推進されています。遺伝学の理解の深化、個別化医療の台頭、そしてバイオテクノロジーの継続的な進歩は、生物製剤を治療研究の最前線へと押し上げる触媒のほんの一部に過ぎません。
フェーズ別:
試験段階別では、世界の臨床試験支援サービス市場において、フェーズIIIが最も大きなシェアを占めており、市場シェアの48%を占めています。この圧倒的な優位性は、医薬品開発パイプラインにおけるフェーズIII試験の重要性に起因しています。これらの試験は、しばしばピボタル試験と呼ばれ、より大規模なコホートを対象とし、対象となる治療の有効性と潜在的な副作用を評価する上で重要な役割を果たします。フェーズIII試験の規模と複雑さを考えると、広範なリソース、モニタリング、そして管理が必要となるため、支援サービスの大きな部分を占めています。.
フェーズIIIの優位性を強めるもう一つの要因は、その規制上の重要性です。このフェーズの成功は、FDAやEMAなどの規制当局による承認取得の礎となることがよくあります。医薬品開発企業は、治験薬がこのフェーズで明確な良好な結果を得ることを目指しているため、フェーズIIIのサポートサービスへの投資は当然ながら高額になります。.
このレポートをカスタマイズ + 専門家による検証
地域別、会社レベル、ユースケース別など、必要なセクションのみにアクセスできます。.
あなたの意思決定を支援するためにドメイン専門家との無料コンサルテーションが含まれています。.
この研究についてさらに詳しく知るには: 無料サンプルをリクエストしてください
サービス別:
サービス分野に焦点を移すと、臨床試験管理セグメントは世界の臨床試験支援サービス市場において際立った存在であり、54%という高い市場シェアを獲得しています。臨床試験管理には、患者募集、治験実施施設の選定、データ管理から規制遵守および報告まで、幅広い必須サービスが含まれます。多面的なプロトコル、多様な患者層、そして厳格な規制要件といった現代の臨床試験の複雑な性質を考えると、効果的な管理は不可欠です。.
臨床試験管理セグメントの優位性は、臨床試験のグローバル化の進展にも起因しています。試験は複数の施設、多くの場合は異なる国や大陸にまたがって実施されるため、統一性と基準遵守を確保するための集中管理の必要性が高まっています。地理的に分散した施設間でシームレスかつ協調的な管理を求める声は、臨床試験管理サービスへの投資と依存を自然に高めています。.
さらに、業界が患者中心のアプローチとリアルワールドデータへと傾倒するにつれ、臨床試験管理のニュアンスが拡大し、世界の臨床試験支援サービス市場におけるこのサービスセグメントの重要性がさらに高まっています。患者のコンプライアンス確保、リアルワールドデータの統合、デジタルツールの活用は、今や臨床試験管理の不可欠な要素となっており、専門的な支援サービスが求められています。.
地域分析
北米は臨床試験支援サービス市場において紛れもないリーダーであり、46.2%という驚異的な収益シェアを占めています。この地域の優位性は、歴史的に画期的な医学研究とイノベーションの中心地であった米国に大きく起因しています。世界的に認められた研究機関や製薬会社が多数拠点を置くこの地域では、臨床研究への多額の資金投資が行われています。例えば、2021年だけでも、米国国立衛生研究所(NIH)は410億ドルを超える資金を医学研究に投入しました。この強固な研究基盤と、米国食品医薬品局(FDA)の厳格な規制要件が相まって、臨床試験のコンプライアンス、効率性、そして品質を確保するために、多岐にわたる専門的な支援サービスが求められています。さらに、精密医療や遺伝子治療といった新たな治療領域の台頭により、この地域における臨床試験数は前年比で推定8%増加しており、支援サービスの需要がさらに高まっています。.
一方、欧州の臨床試験支援サービス市場は、臨床試験支援サービス分野で26%以上の市場シェアを占め、重要なプレーヤーとしての地位を維持しています。欧州は、人口動態や患者層の多様性に富み、より一般的な結果を目指す臨床試験に独自の優位性を提供しています。2021~2022年度には、ドイツ、フランス、英国などの国々で臨床研究への投資が合計150億ユーロに達し、この地域の医学の発展への取り組みが示されました。欧州の魅力は、欧州医薬品庁(EMA)と加盟国間の規制調和に向けた一貫した取り組みによってさらに高まっています。こうした取り組みにより、かつてこの地域における複数国での試験に伴う官僚的なハードルが大幅に軽減されました。その結果、欧州における臨床試験支援サービスの需要は、年間約6%の安定した成長を遂げています。.
世界の臨床試験支援サービス市場におけるトッププレーヤー
- チャールズリバーラボラトリーズ
- コーヴァンス社.
- アイコンPLC
- inVentiv International Pharma Services
- アイクビア
- ラボラトリー・コーポレーション・オブ・アメリカ・ホールディングス
- ノボテック
- パレクセルインターナショナル
- 製薬製品開発LLC
- クォーティエント・バイオリサーチ
- 無錫AppTec
- 白血病・リンパ腫協会(LLS)
- その他の著名な選手
市場セグメンテーションの概要:
トライアルの種類別
- 集中臨床試験
- 分散型臨床試験
治療の種類別
- 小さな分子
- 生物学的製剤
- 医療治療の種類
フェーズ別
- 前臨床研究
- フェーズI
- フェーズII
- フェーズIII
- フェーズIV
サービス別
- サイト管理
- 患者募集
- 臨床試験管理
- データ管理
- その他
アプリケーション別
- 腫瘍学
- 中枢神経系および精神障害
- 心血管疾患
- 感染症
- 血液疾患
- その他
エンドユーザー別
- 製薬・バイオテクノロジー企業
- 契約研究機関(CRO)
- 医療治療の種類企業
- その他
地域別
- 北米
- 米国
- カナダ
- メキシコ
- ヨーロッパ
- 英国.
- ドイツ
- フランス
- スペイン
- ポーランド
- ベルギー
- フィンランド
- オランダ
- ポルトガル
- スウェーデン
- スイス
- その他のヨーロッパ
- アジア太平洋
- 中国
- インド
- 日本
- オーストラリアとニュージーランド
- ASEAN
- 韓国
- その他のアジア太平洋地域
- 中東・アフリカ
- アラブ首長国連邦
- サウジアラビア
- カタール
- 南アフリカ
- モロッコ
- MEAの残りの地域
- 南アメリカ
- ブラジル
- アルゼンチン
- コロンビア
- チリ
- ペルー
- 南アメリカのその他の地域
レポートの範囲
| レポート属性 | 詳細 |
|---|---|
| 2023年の市場規模価値 | 252億米ドル |
| 2032年の予想収益 | 471億米ドル |
| 履歴データ | 2019-2022 |
| 基準年 | 2023 |
| 予測期間 | 2024-2032 |
| ユニット | 価値(10億米ドル) |
| 年平均成長率 | 7.22% |
| 対象セグメント | 試験タイプ別、治療タイプ別、フェーズ別、サービス別、アプリケーション別、エンドユーザー別、地域別 |
| 主要企業 | Charles River Laboratories、Covance Inc.、Icon PLC、inVentiv International Pharma Services、IQVIA、Laboratory Corp. of America Holdings、Novotech、Parexel International、Pharmaceutical Product Development LLC、Quotient Bioresearch、WuXi AppTec、白血病リンパ腫協会(LLS)、その他の著名な企業 |
| カスタマイズ範囲 | ご希望に応じてカスタマイズされたレポートを入手してください。 カスタマイズをリクエストしてください |
包括的な市場知識をお探しですか? 当社の専門スペシャリストにご相談ください。.
アナリストに相談する
.svg)