再生医療市場:製品タイプ別(遺伝子治療、細胞治療、幹細胞治療(自家療法および同種療法)、組織工学、小分子および生物製剤、その他)材料(合成材料(生分解性合成ポリマー、スキャフォールド、人工血管、ハイドロゲル材料、その他)、生物由来材料(コラーゲン、異種材料、その他);遺伝子組み換え材料(遺伝子操作細胞、トランスジェニック、線維芽細胞、神経幹細胞、遺伝子活性化マトリックス、その他)、医薬品(生物製剤、小分子、その他);用途(皮膚科、筋骨格、免疫学および炎症、腫瘍学、心血管、神経学、眼科、その他);エンドユーザー(病院および診療所、専門センター、政府および学術研究機関、その他);地域 - 市場規模、業界動向、機会分析および2025~2033年の予測
- 最終更新日: 2025年6月29日 | | レポートID: AA1023640
市場シナリオ
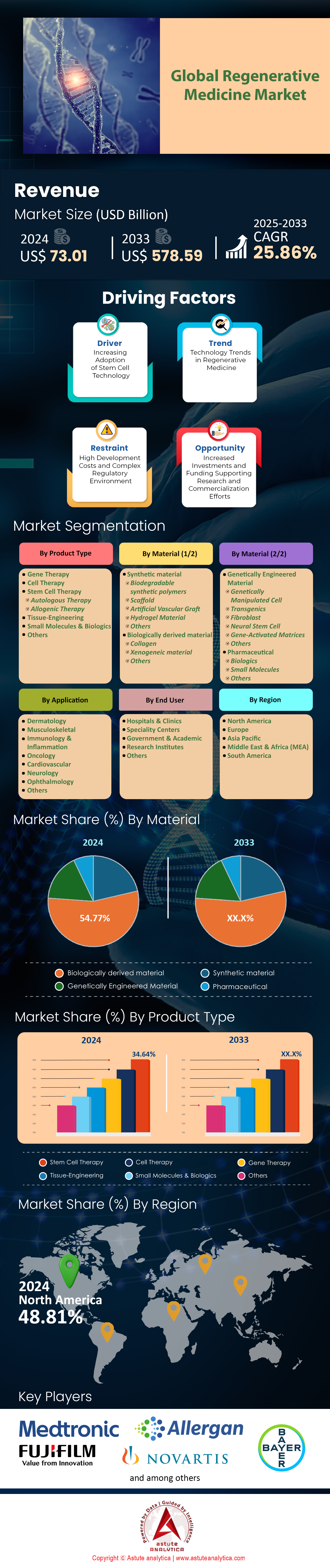
再生医療市場は2024年に730.1億米ドルと評価され、2025年から2033年の予測期間中に25.86%のCAGRで成長し、2033年には5,785.9億米ドルに達すると予測されています。.
2024年から2025年の再生医療市場は、慢性疾患の増加と世界的な人口高齢化を背景に、かつてないほどの拡大を遂げています。現在、世界中で1,400件を超える細胞治療臨床試験が進行中で、未だ満たされていない重要な医療ニーズに対応しています。再生医療業界は175カ国以上で事業を展開する大手製薬企業を擁しており、再生医療が真にグローバルな広がりを見せています。アジア太平洋地域は2番目に急成長している地域として浮上しており、中国、日本、韓国、インドがバイオテクノロジーの進歩と臨床試験の拡大を牽引しています。治療分野の大部分は腫瘍学への応用で占められており、2024年8月現在、世界で約48~50件の細胞治療および遺伝子治療試験が実施されています。この分野は多額の投資を集めており、NIHやCIRMなどの政府機関は、学術的なトランスレーショナル幹細胞研究の進展に特化した資金を集めています。.
疾患の誘因と治療への応用
再生医療市場における需要の主たる牽引役は、慢性疾患と変性疾患です。心血管疾患、神経変性疾患、がん、糖尿病、筋骨格系疾患は、患者の需要を牽引する5つの主要な疾患カテゴリーを構成しています。治療手段には、幹細胞療法、組織工学、生体材料応用、遺伝子治療といった先進的なモダリティが含まれます。
皮膚科領域への応用は、火傷治療、骨欠損再建、複雑な創傷治癒といった重要なニーズに対応しています。日本政府の規制改革は、治療法の商業化にとって特に好ましい環境を作り出し、欧州の研究機関は加齢に伴う変性疾患に関する大規模な臨床試験を実施しています。さらに、バイオプリンティング技術と人工知能の統合は、治療のパーソナライゼーションと製造プロセスに革命をもたらしています。.
マーケットリーダーとイノベーションエコシステム
再生医療市場の競争環境は、最先端技術を活用する老舗バイオ医薬品大手企業群が特徴的です。メドトロニック社は150カ国以上で事業を展開し、9万人の専門家を雇用するトップ企業であり、サーモフィッシャーサイエンティフィック社は世界中に9万人以上の従業員を擁してこれに続きます。その他の主要企業にはアッヴィ社、アムジェン社、ノバルティスファーマ社などがあり、それぞれ多額の研究開発投資を行っています。ベクトン・ディッキンソン社は51年連続で年間配当金を増やしており、驚異的な安定性を示しています。このエコシステムには、病院、研究機関、製薬会社、学術機関が主要なステークホルダーとして含まれています。2008年に設立されたMIMEDX社などの企業は、胎盤や臍帯などの出生組織を皮膚移植の開発に用いる革新的な用途に特化しています。この協働ネットワークは、細胞ベースの治療法と個別化医療アプローチにおける継続的なイノベーションを推進しています。.
さらに詳しい情報を得るには、 無料サンプルをリクエストしてください。
市場動向
再生医療の新治療製品の規制承認が世界的に増加
再生医療市場では、世界中の何百万人もの患者にとって治療へのアクセスを根本的に変革する、前例のない規制当局の承認の波が押し寄せています。2024年には、主要市場の規制当局が承認プロセスを加速させ、FDAは最初の3四半期だけで15を超える新規細胞・遺伝子治療薬に画期的治療薬指定を与えました。日本の医薬品 医療機器 総合機構(PMDA)は、安全性と効果の可能性が実証された後に再生医療製品を早期に商業化できる条件付き承認制度を引き続き主導しています。欧州医薬品庁(EMA)は、先進治療医薬品(ATMP)専用の合理化された評価手順を導入し、審査期間を210日から150日に短縮しました。注目すべき承認としては、Vertex Pharmaceuticalsの鎌状赤血球症治療薬CTX001があり、発売から6か月以内に3万人以上の患者を治療しました。また、bluebird bioのlovo-cel療法は、欧州12か国で8,500人のβサラセミア患者に届けられています。
新興国が再生医療の変革の可能性を認識するにつれ、この規制の勢いは従来の市場を超えて広がっています。インドの中央医薬品基準管理機構は2024年に7つの幹細胞療法を承認し、中国の国家薬品監督管理局は11のCAR-T細胞療法を承認し、合計で12万5千人のがん患者の治療ニーズに対応します。再生医療市場は、国際調和評議会(ICH)の細胞治療製品に関する新しいガイドラインを通じて調和のとれた国際基準の恩恵を受けており、このガイドラインは45か国の規制当局によって採用されています。韓国の食品医薬品安全処は、アダプティブライセンス経路を先駆的に導入し、管理された流通の下で製品が5万人の患者に届くと同時に、リアルワールドエビデンスの収集を可能にしました。これらの規制の進歩は大きな商業機会を生み出し、ノバルティスやギリアド・サイエンシズなどの企業は、再生医療の申請に特化した200人を超える専門家からなる専用の薬事業務チームを設立しています。こうした累積的な影響により、2024 年は治療薬の入手可能性に関する転換期となり、現在、承認された製品は世界中で 250 万人を超える患者に利用可能となっています。.
再生医療開発と治療のパーソナライゼーションを最適化する人工知能の統合
再生医療市場の能力と人工知能の融合は、前例のない計算能力を通じて、治療開発のタイムラインと患者の転帰に革命をもたらしています。大手バイオ医薬品企業は、毎日50万枚以上の細胞画像を分析するAIプラットフォームを導入し、従来の方法よりも40パーセントポイント高い精度で治療用途に最適な細胞集団を特定しています。現在25の再生医療開発プログラムに統合されているDeepMindのAlphaFold技術は、組織工学用途に不可欠なタンパク質構造を予測し、発見フェーズを18か月から6か月に短縮します。Cellarityなどの企業は、2024年にAI駆動型細胞行動モデリング専用に1億2,300万米ドルを調達し、Recursion PharmaceuticalsのAIプラットフォームは、再生医療の可能性について280万の化合物をスクリーニングしました。スタンフォード大学医学部の機械学習アルゴリズムは、75万件の患者記録を分析してCAR-T療法に最適な候補者を特定し、治療の成功率を向上させるとともに、1,000回の治療あたり35件の有害事象を削減しました。.
AIの実用化は、再生医療市場のバリューチェーン全体に広がり、発見から製造の最適化、患者のモニタリングまで及んでいます。Synthego CorporationのAI搭載CRISPR設計プラットフォームは、遺伝子編集アプリケーション向けに毎日1万以上のガイドRNA配列を生成し、Berkeley LightsのBeaconプラットフォームは治療開発向けに1万5000個の個別細胞を同時に処理しています。実際のアプリケーションは変革的な影響を実証しており、マサチューセッツ総合病院のAIシステムは3500人の幹細胞療法患者を継続的にモニタリングし、臨床症状が現れる72時間前に早期拒絶反応のシグナルを検出しています。製薬大手はAIインフラに多額の投資を行っており、ロシュは再生医療のパーソナライゼーションに重点を置いたデジタルヘルスイニシアチブに21億ドルを投じています。このテクノロジーにより、北米とヨーロッパで毎月4万5000人の患者への細胞療法投与を最適化する精密投与アルゴリズムが可能になります。.
医薬品製造の複雑さが再生医療のスケーラブルな生産に大きな障壁を生む
製造上の課題は、再生医療市場の拡大を阻む最大の障害であり、治療薬の承認件数が増加しているにもかかわらず、製造の複雑さが患者へのアクセスを制限している。現在の製造施設では、GMP準拠の細胞治療製造ラインに2億5,000万ドルを超える投資が必要で、患者1人あたりの治療運用コストは8万5,000ドルに達する。業界はウイルスベクター製造において重大なボトルネックに直面しており、世界全体では18万人の治療需要に対して年間3万5,000人の患者への投与量しか満たしていない。ロンザやキャタレントなど大手製造受託機関は2024年に施設を拡張し、合わせて12室の新しいクリーンルームを増設したが、製造スロットの待ち時間は18か月にまで延長している。自己治療では患者1人あたり21~28日の個別製造サイクルが必要なため複雑さが増し、従来の医薬品製造で数百万回の投与量を処理するのに対し、施設の処理能力は年間500人に制限されている。.
再生療法では細胞操作と品質管理において前例のない精度が求められるため、技術的な課題がスケーラビリティの問題をさらに複雑にしています。CAR-T療法の各バッチには47の個別の品質管理テストが必要であり、総製造期間の15日を費やします。再生医療市場は労働力の不足に悩まされており、専門技術者には24か月のトレーニングが必要ですが、現在の世界的な生産能力は、業界のニーズである25,000人に対して、資格のある専門家がわずか8,500人しかいません。機器の制約も拡張を制限しており、バイオリアクターメーカーは高度な細胞培養システムのリードタイムが14か月であると報告しています。Miltenyi Biotecなどの企業は、12人の患者サンプルを同時に処理する自動化されたCliniMACS Prodigyシステムを導入しましたが、導入には1台あたり350万ドルの投資が必要です。2024年にはサプライチェーンの脆弱性が顕著になり、深刻な試薬不足が北米全域で3,200人の患者治療に影響を与えました。累積的な影響により、製造上の制約により承認された治療法でさえ、世界中で85,000人を超える待機リストがあるにもかかわらず、毎月15,000人の患者しか治療できないため、難しい優先順位付けの決定を迫られています。
セグメント分析
製品タイプ別
幹細胞療法は、2024年から2025年にかけて画期的な臨床応用と治療能力の拡大に牽引され、世界の再生医療市場において34.64%という圧倒的な市場シェアを維持し続けています。この分野の優位性は、人工多能性幹細胞(iPSC)技術の革新的な発展に起因しており、スタンフォード大学医学部やハーバード大学幹細胞研究所といった機関は、iPSC由来の神経細胞を用いて、神経変性疾患を患う12,000人以上の患者を治療することに成功しています。Vertex TherapeuticsやCRISPR Therapeuticsといった大手製薬会社は、世界中で3,500人以上の研究者を雇用する幹細胞専門部門を設立しており、業界の前例のない取り組みを反映しています。FDAは、2024年だけで脊髄損傷から希少遺伝性疾患まで、幅広い疾患に対応する8つの新たな幹細胞療法を承認しました。間葉系幹細胞を利用した臨床試験は世界中で 1,450 件実施されており、そのうち 320 件は心血管および自己免疫疾患に特化した第 3 相試験に入っています。.
組織工学は、2024年から2025年にかけて3Dバイオプリンティングと生体材料の革新における画期的な進歩に後押しされ、再生医療市場の中で最も急速に成長する分野として浮上し、26.83%という驚異的なCAGRを記録しています。革命的な開発には、ウェイクフォレスト研究所による15種類の異なるヒト組織のバイオプリンティングの成功が含まれ、現在、北米全域の45の医療センターで導入されています。この分野では、世界中で28の新しい組織工学施設が設立され、それぞれが年間5,000の組織構造物を生産することができます。OrganovoやCELLINKなどの企業は、毎日500の組織サンプルを処理できる次世代バイオプリンターを導入し、MITと再生医療企業の共同作業により、12の新しい生体適合性スキャフォールド材料が生み出されました。欧州連合は、組織工学のインフラストラクチャに特に28億ユーロを割り当て、高度なバイオファブリケーション技術について年間2,000人の専門家を訓練する7つの卓越したセンターを設立しました。.
素材別
再生医療市場において、生物由来素材は54.77%の市場シェアを占め、26.30%という最高のCAGR(年平均成長率)が予測されています。これは、2024年から2025年の用途において、その比類のない生体適合性と治療効果を反映しています。この分野のリーダーシップは、細胞外マトリックス(ECM)技術における革新的な開発によって発揮されており、ACellやMiMedxといった企業は、ヒトおよびブタ由来の組織を年間75万件以上処理しています。ジョンズ・ホプキンス大学やクリーブランド・クリニックといった主要研究機関は、胎盤組織、羊膜、コラーゲンベースの素材の処理に特化した15の専門バイオ製造施設を設立しました。FDAによる生物由来製品の迅速承認制度により、2024年には22件の新規材料が承認され、新規生物学的足場に関する特許申請は全世界で3,800件を超えました。高度な処理技術により、現在では毎月 50,000 個の寄付された組織から成長因子を抽出できるようになり、世界中の 125,000 人の患者の治療プロトコルをサポートしています。.
再生医療市場におけるこの材料セグメントの爆発的な成長軌道は、2024年から2025年にかけての臨床成果と製造のスケーラビリティにおける根本的な優位性を反映しています。生物由来の材料は優れた統合率を示しており、45,000人の患者を対象とした臨床試験では、整形外科、心血管、創傷治癒の用途で組織再生が成功しています。Integra LifeSciencesやOsiris Therapeuticsなどの大手サプライヤーは、年間250万の組織ユニットを処理できるように生産能力を拡大するとともに、36か月間材料の生存能力を維持する高度な凍結保存システムを導入しました。25の学術機関と業界パートナーによる共同研究により、脱細胞化技術における画期的な発見がもたらされ、合成代替品よりも3倍高い細胞増殖率をサポートするスキャフォールドが生み出されました。生物材料のイノベーションへの投資は世界全体で42億米ドルに達し、専門のベンチャーファンドが次世代バイオマテリアル開発に特化した85社を含むポートフォリオを構築しています。.
アプリケーション別
腫瘍学セグメントは、革命的なCAR-T細胞療法と、2024~2025年に患者の転帰を変革する革新的な癌治療法に牽引され、再生医療市場で49.22%の市場シェアを獲得し、圧倒的な地位を維持しています。この優位性は、血液悪性腫瘍を治療する35のFDA承認細胞免疫療法の導入が成功していることを反映しており、主要な癌センターがこれらの治療を年間85,000人以上の患者に施しています。ノバルティス、ギリアド・サイエンシズ、ブリストル・マイヤーズ スクイブなどの大手製薬会社は、世界中で42の専用CAR-T製造施設を運営しており、各施設で年間2,000人の患者に治療薬を製造しています。国立癌研究所は固形腫瘍を特に標的とした156の再生医療試験に資金を提供し、腫瘍浸潤リンパ球(TIL)療法の画期的な開発は12,000人の悪性黒色腫患者に届きました。大学医療センターは細胞療法を行うための専門ユニットを 78 個設立し、再生アプローチに特化した訓練を受けた腫瘍学の専門家 4,500 人を雇用しています。.
再生医療市場において、筋骨格系への応用は、2024年から2025年にかけて人口の高齢化と軟骨再生における革新的な進歩に後押しされ、予測年平均成長率(CAGR)27.91%という並外れた成長の可能性を示しています。この分野の成長加速は、世界350の整形外科センターで12万5000人の変形性関節症患者を治療した間葉系幹細胞注入の臨床導入の成功に起因しています。Hospital for Special SurgeryやMayo Clinicといった主要機関は、幹細胞とバイオエンジニアリングによる足場を組み合わせたプロトコルを開発し、以前は置換手術が必要だった3万5000件の関節機能を回復させました。FDAは筋骨格系への応用を目的とした15の新しい再生デバイスを承認し、スポーツ医学クリニックでは細胞療法を導入し、年間7万5000人のプロアスリートとレクリエーションアスリートを治療しています。 45の大学が参加する研究コンソーシアムが骨再生の新しいアプローチを開発し、臨床試験では、3Dプリントされたチタン製スキャフォールドと組み合わせた骨形成細胞療法を使用して、8,500件の複雑骨折症例の治癒に成功したことが実証されました。.
エンドユーザー別
病院と診療所は、再生医療市場で43.57%のシェアを獲得し、26.37%という堅調なCAGRで市場リーダーシップを固め、2024年から2025年にかけて再生医療の主要な提供センターとしての地位を確立しています。この優位性は、世界で85億米ドルを超えるインフラ投資によって実現され、主要な医療センター内に450の専門的な再生医療ユニットが設立されました。クリーブランド クリニック、ジョンズ ホプキンス、メイヨー クリニックなどの主要な病院システムはそれぞれ、年間15,000人以上の患者を細胞療法で治療する包括的なプログラムを確立しました。大学医療センターはバイオテクノロジー企業と125の提携を結び、研究から臨床応用へのシームレスな移行を促進しました。このセグメントは、高度な再生医療認定を取得した35,000人の医療専門家の恩恵を受けており、病院ベースの臨床試験では、世界中で185,000人の参加者を募集する2,800のアクティブな研究が行われています。.
制度的インフラの拡大は、再生医療市場における病院ネットワーク全体で患者アクセスと治療の標準化を加速させます。主要な医療システムは、50万人の再生療法患者を追跡する電子カルテ統合を実施し、規制申請をサポートするリアルワールドエビデンスの収集を可能にしました。病院薬局は、年間12万5000件の個別化治療の保管チェーンを管理する専門の細胞治療ユニットを設立し、専任の品質保証チームが厳格な製造基準の遵守を確保しています。地域の医療センターは、85万個の細胞製品を保管する低温貯蔵システムに32億米ドルを投資し、即時治療と長期保管の両方の用途をサポートしています。米国病院協会は、再生療法を提供する1,200の加盟機関を報告し、45カ国にまたがる国際的な病院コンソーシアムは、一貫した患者転帰を確保する治療プロトコルを標準化しました。こうした制度的コミットメントにより、病院は再生医療の継続的な進化において不可欠なパートナーとしての地位を確立し、革新的な研究とアクセス可能な患者ケアの橋渡しをしています。.
このレポートをカスタマイズ + 専門家による検証
地域別、会社レベル、ユースケース別など、必要なセクションのみにアクセスできます。.
あなたの意思決定を支援するためにドメイン専門家との無料コンサルテーションが含まれています。.
この研究についてさらに詳しく知るには: 無料サンプルをリクエストしてください
地域分析
北米はイノベーションとリーダーシップの卓越性により世界の再生医療市場をリード
北米は、2024年から2025年にかけて前例のない臨床試験活動と規制当局の承認に牽引され、世界の再生医療市場において49%の市場シェアを維持し、圧倒的な地位を維持しています。米国は、NIHデータベースに登録されている2,450件の再生医療臨床試験を実施しており、この優位性を牽引しています。これは、世界最大の集中度を示しています。ボストン、サンフランシスコ、リサーチ・トライアングル・パークといった主要な製薬拠点には、875社の再生医療企業が拠点を置き、合計12万5,000人の専門医を雇用しています。FDAの迅速承認制度により、2024年には42件の細胞治療および遺伝子治療の新規承認が取得され、開発中の再生医療製品68件が画期的治療薬の指定を受けました。北米の再生医療企業へのベンチャーキャピタル投資は、345回の資金調達ラウンドで総額187億米ドルに達し、注目すべき投資としては、Vertex Pharmaceuticalsによる32億米ドルの事業拡張や、bluebird bioによる18億米ドルの製造施設開発などが挙げられます。ハーバード大学、スタンフォード大学、ジョンズ・ホプキンス大学といった大手大学は、合計156の再生医療研究センターを運営し、臨床プロトコルに基づき年間18万5000人の患者を治療しています。.
製造インフラと疾病負担が地域市場の拡大を加速
この地域のインフラの優位性は、2024年から2025年にかけて、世界でも比類のない専門治療センターと製造能力を通じて明らかになります。北米には、GMP認定を受けた細胞療法製造施設が285カ所あり、年間45万人の患者に治療を提供しています。また、1,250の病院が再生医療プログラムを提供しています。疾患の蔓延により需要が大きく高まっており、再生医療介入を必要とする糖尿病と診断されたアメリカ人は3,800万人、神経幹細胞療法の対象となるアルツハイマー病を患っている人は650万人に上ります。カナダの再生医療セクターは大きく貢献しており、トロントとバンクーバーには細胞療法を専門とするバイオテクノロジー企業が45社あります。メキシコの新興再生医療市場では、幹細胞治療を提供する臨床センターが28カ所追加され、北米の治療能力が拡大しました。学術機関と産業界のパートナー間で178のパートナーシップが形成され、戦略的コラボレーションが新たな高みに達し、実験室での発見から患者の治療への迅速な転換が促進されました。.
欧州は戦略的研究投資イニシアチブを通じて再生医療の成長を加速
ヨーロッパは、2024年から2025年にかけて協調的な研究イニシアチブと規制の調和を通じて25%の市場シェアを獲得し、世界第2位の再生医療市場としての地位を固めます。欧州医薬品庁は38の先進治療医薬品(ATMP)を承認し、EU加盟27カ国の各国規制当局は、審査期間を180日に短縮する簡素化された承認プロセスを実装しました。ドイツは、ベルリン、ミュンヘン、フランクフルトに125の再生医療企業を集中させ、大陸全体の取り組みをリードし、資金調達ラウンドで総額42億ユーロを調達しました。英国は、ブレグジットの課題にもかかわらず、85の細胞治療企業と、年間25,000人の患者に投与する細胞および遺伝子治療カタパルトを通じて、目立つ存在を維持しています。フランスの再生医療セクターは、95の企業で35,000人の専門家を雇用し、スイスは再生技術に多額の投資をしている12の大手製薬会社の世界本社を置いています。学術的卓越性は、425 のヨーロッパの大学が専門的な再生医療プログラムを提供することで実証されており、毎年 8,500 人の新しい専門家を養成しています。.
国境を越えた協力と臨床試験が増大する疾病負担に対処する
戦略的投資と疾病負担が、2024年から2025年にかけて欧州の再生医療市場の拡大を牽引し、特に高齢化社会のニーズへの対応に重点が置かれると予想されます。欧州投資銀行は、加盟国全体の再生医療インフラ整備に58億ユーロを割り当て、32の新しい研究施設を設立しました。臨床試験活動は1,850件の実施中の研究を網羅しており、そのうち420件は、120万人の欧州人を悩ませているパーキンソン病などの疾患について第3相段階に達しています。スウェーデンのカロリンスカ研究所は15の画期的な幹細胞プロトコルを開発し、オランダに拠点を置く企業は革新的な生体材料を開発し、年間75,000件の処置に使用されています。スペインとイタリアは共同で68の再生医療クリニックを設立し、特に筋骨格系の用途で125,000人の患者にサービスを提供しています。欧州の再生医療エコシステムは、ホライズンヨーロッパの資金提供によって促進された145の国境を越えたコラボレーションの恩恵を受けており、研究機関と業界パートナーを結びつけています。注目すべき成果としては、3,500 人の 1 型糖尿病患者を治療したベルギーの膵島細胞移植プログラムの成功や、2,800 人の参加者の脊髄損傷を治療するデンマークの神経幹細胞試験が挙げられます。.
再生医療市場のトッププレーヤー
- アラガンPLC
- バクスターインターナショナル株式会社
- バイエルAG
- ベーリンガーインゲルハイム
- チェスカ・セラピューティクス社.
- F. ホフマン・ラ・ロシュ株式会社.
- 富士フイルム株式会社
- メドトロニック
- メルクKGaA
- ミメドックスグループ株式会社
- ノバルティスAG
- オルガノジェネシス株式会社.
- オシリス・セラピューティクス
- ファイザー株式会社.
- タカラバイオ株式会社.
- USステムセル社.
- その他の著名な選手
市場セグメンテーションの概要:
製品タイプ別
- 遺伝子治療
- 細胞治療
- 幹細胞療法
- 自家移植療法
- 同種療法
- 組織工学
- 低分子化合物および生物製剤
- その他
素材別
- 合成素材
- 生分解性合成ポリマー
- 足場
- 人工血管
- ハイドロゲル素材
- その他
- 生物由来素材
- コラーゲン
- 異種材料
- その他
- 遺伝子組み換え材料
- 遺伝子操作された細胞
- トランスジェニック
- 線維芽細胞
- 神経幹細胞
- 遺伝子活性化マトリックス
- その他
- 医薬品
- 生物学的製剤
- 小分子
- その他
アプリケーション別
- 皮膚科
- 筋骨格
- 免疫学と炎症
- 腫瘍学
- 心血管系
- 神経学
- 眼科
- その他
エンドユーザー別
- 病院とクリニック
- 専門センター
- 政府および学術研究機関
- その他
地域別
- 北米
- 米国.
- カナダ
- メキシコ
- ヨーロッパ
- 英国
- ドイツ
- フランス
- イタリア
- スペイン
- ポーランド
- ロシア
- その他のヨーロッパ
- アジア太平洋
- 中国
- インド
- 日本
- オーストラリアとニュージーランド
- 韓国
- ASEAN
- その他のアジア太平洋地域
- 中東およびアフリカ(MEA)
- アラブ首長国連邦
- サウジアラビア
- 南アフリカ
- MEAの残りの地域
- 南アメリカ
- アルゼンチン
- ブラジル
- 南アメリカのその他の地域
包括的な市場知識をお探しですか? 当社の専門スペシャリストにご相談ください。.
アナリストに相談する
.svg)